- Процесс заряда аккумуляторов различных типов
- Заряд аккумуляторов различных типов
- Свинцово-кислотные АКБ
- Происходящие процессы
- Режимы заряда
- Щелочные аккумуляторные батареи
- Происходящие процессы
- Режимы заряда
- Литиевые
- Происходящие процессы
- Режимы заряда
- Как предотвратить взрыв водорода в тяговом аккумуляторе
- Почему образуется водород
- Что усиливает выделение водорода
- Как происходит взрыв
Процесс заряда аккумуляторов различных типов
Заряд и разряд аккумулятора являются основными процессами, которые идут при его эксплуатации. Во время заряда аккумуляторная батарея восполняет потерянную ёмкость и по окончании процесса вновь может эксплуатироваться. В этом материале речь пойдёт о заряде аккумуляторов основных типов: свинцово-кислотных, щелочных и литиевых. Будут рассмотрены процессы происходящие при зарядке и режимы.
Заряд аккумуляторов различных типов
Свинцово-кислотные АКБ
Самой распространённой сферой применения свинцово-кислотных аккумуляторов, являются стартерные батареи в транспортных средствах. Они применяются для запуска двигателя, а также поддержки генератора при сильной нагрузке на бортовую сеть автомобиля. В штатном режиме работы свинцово-кислотные АКБ не испытывают глубокого разряда. Заряд батареи после пуска осуществляется током, вырабатываемым генератором. Кроме того, рекомендуется периодически выполнять зарядку стартерного аккумулятора от зарядного устройства. Какие реакции при этом происходят?

Происходящие процессы
В электрохимической реакции внутри свинцово-кислотного аккумулятора участвуют материалы положительного и отрицательного электрода, а также электролит. Активная масса положительного электрода представляет собой диоксид свинца (PbO2). В случае с отрицательным электродом – это порошок свинца (Pb). При заряде свинцово-кислотной аккумуляторной батареи на электродах протекают следующие реакции.
Общий процесс в электрохимической системе описывается уравнением.
В процессе заряда из электролита расходуется вода и постепенно увеличивается его плотность. Плотность электролита полностью заряженного аккумулятора находится около 1,27 гр/см 3 . Ниже можно посмотреть таблицу степени заряженности АКБ.
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
|---|---|---|---|---|
| 1,11 | 11,7 | 8,4 | 0 | -7 |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,27 | 12,66 | 10,8 | 100 | -60 |
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
Основной проблемой в процессе заряда свинцово-кислотного аккумулятора является неполное растворение сульфата свинца (PbSO4). Это вещество забивает поры активной массы, в результате чего снижается площадь взаимодействия электролита с материалом электрода. Из-за этого происходит постепенная потеря ёмкости.
По мере эксплуатации аккумуляторной батареи сульфата свинца на пластинах после заряда остаётся всё больше. Процесс носит название сульфатации. Он является причиной выхода из строя большинства свинцово-кислотных аккумуляторов на транспортных средствах.
Режимы заряда
Если не считать ускоренной зарядки, то есть две основные схемы заряда свинцово-кислотных аккумуляторных батарей. При постоянном напряжении и постоянном токе. Сегодня в продаже можно найти много зарядных устройств (ЗУ), имеющих возможность использования этих режимов, а также их комбинаций.
Наиболее распространённой является схема заряда при постоянном напряжении. Смысл здесь в том, что на терминалы аккумулятора подаётся постоянное напряжение. Заряд обеспечивается благодаря выравниванию напряжений на выводах ЗУ. Полнота заряда в этом случае зависит от напряжения, подаваемого на только выводы АКБ. То есть если заряжать аккумуляторную батарею одинаковое время напряжением 14,4, 15 и 16 вольт, то наиболее полный заряд достигается при 16 В.

Другой распространённой схемой является заряд постоянным током. Этот процесс включает в себя несколько этапов, на каждом из которых поддерживается постоянная сила тока.
Такая схема зарядки требует постоянного контроля и корректировки подаваемого тока. Этапы разделяются по уровню напряжения на выводах аккумулятора.
Обычно процесс выглядит следующим образом.
- На первом этапе сила тока устанавливается в размере 10% от номинальной ёмкости АКБ. После этого проводится зарядка до постоянного напряжения 14,4 вольта.
- Второй этап начинается с напряжения 14,4 вольта. Это значение является тем уровнем, на котором начинается разложение воды из электролита на кислород и водород. У аккумуляторов, выпускаемых по технологии Ca-Ca, это значение напряжения выше. Чтобы минимизировать выделение газов, сила тока снижается в два раза. То есть если на первом этапе она была 5 ампер, то здесь нужно уменьшить до 2,5 А.
- Третий этап стартует с напряжения 15 вольт. Сила тока уменьшается два раза по сравнению со вторым этапом. Далее через определённые промежутки времени (1─2 часа) проверяется напряжение на терминалах. Как только оно перестаёт меняться, так можно считать процесс оконченным. На последнем этапе будет идти активное выделение газов. По этой причине аккумуляторная батарея должна находиться в хорошо проветриваемом помещении, а рядом не должно быть искр и открытого пламени.
Выше был упомянут метод ускоренной зарядки аккумуляторной батареи. Подобный режим есть во многих зарядных устройствах. Он отличается лишь тем, что на аккумулятор подаётся увеличенный до 30% (по сравнению со штатным значением 0,1*С) ток. Это используется в тех случаях, когда аккумулятору нужно быстро отдать заряд, который необходим для запуска двигателя. Увеличенная сила тока при зарядке отрицательно сказывается на состоянии электродов и активной массы. Поэтому без необходимости этот режим лучше не использовать.
Щелочные аккумуляторные батареи
Щелочные аккумуляторы используются в качестве тяговых. Их можно встретить в различной складской технике, железнодорожном транспорте, электроинструменте и других сферах применения, где они работают в режиме циклирования.

Происходящие процессы
Наиболее распространёнными электрохимическими системами щелочных аккумуляторов являются никель─кадмиевые и никель─металлогидридные. Рассмотрим процесс заряда на их примере. Оба типа батарей имеют положительный электрод с активной массой из гидроокиси никеля (NiOOH). В ней присутствует графит и окись бария. Окись бария продлевает срок службы АКБ, а графит увеличивает электропроводность активной массы.
Активная масса на отрицательном электроде в никель─кадмиевых аккумуляторах представляет собой смесь порошков кадмия (Cd) и железа (Fe). У никель─металлогидридных аккумуляторов активная масса на минусовом электроде является смесью порошков железа и его окислов. В неё добавляют сернокислый никель (NiSO4) и сернистое железо (FeS).
Ниже представлены реакции, происходящие в щелочном аккумуляторе при заряде.
2Ni(OH)2 + 2KOH + Fe(OH)2 -> 2Ni(OOH) + 2KOH + Fe
2Ni(OH)2 + 2KOH + Cd(OH)2 -> 2Ni(OOH) + 2KOH + Cd
В процессе разряда активная масса на положительном электроде окисляется и 2Ni(OH)2 превращается в гидроокись никеля. Одновременно с этим в активной массе отрицательного электрода происходит восстановление, в результате которого образуется железо и кадмий.
Режимы заряда
Если рассматривать заряд стандартного аккумуляторного элемента Ni-Cd, то рекомендуемый ток составляет 10─20% от номинальной ёмкости. Во время зарядки может доходить до 16 часов. Допустимый диапазон температур для зарядки щелочных аккумуляторов составляет от 0 до 50 по Цельсию. Наиболее эффективно процесс заряда происходит в диапазоне температур от 10 до 40 градусов Цельсия.
На практике конструкция щелочных аккумуляторов позволяет заряжать их током не менее 30% от номинальной ёмкости. Процесс заряда в этом случае занимает несколько часов. При заряде щелочных аккумуляторов есть один важный момент. Особенно это актуально для никель─кадмиевых батарей. Они имеют такую проблему, как «эффект памяти». Поэтому перед зарядом эти АКБ требуется разрядить. Подобным функционалом располагают многие зарядные устройства, предназначенные для работы со щелочными аккумуляторами.
Поэтому процесс зарядки щелочного аккумулятора чаще всего начинается с его разряда. При этом не должно допускаться снижение напряжения на выводах элемента ниже 1 вольта. После разряда запускается процесс заряда.
Различных схем заряда для щелочных батарей значительно больше, чем для свинцово-кислотных. Некоторые из них приведены на изображении ниже.
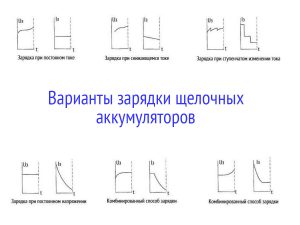
В процессе заряда напряжение на выводах щелочного аккумулятора постепенно увеличивается до 1,6─1,75 вольта. На заключительном этапе напряжение может подниматься до 1,8 вольта. В случае с герметичными щелочными АКБ бывает так, что окончание заряда определяется переданными ампер-часами. Чтобы зарядить батарею целиком иногда расходуется количество энергии, соответствующее 150 процентам от номинальной ёмкости. Напряжение полностью заряженного щелочного аккумулятора в разомкнутой цепи составляет 1,45 вольта.
Вернуться к содержанию
Литиевые
Процесс заряда будет рассмотрен на примере литий─ионных аккумуляторных батарей. В последнее время они получили широкое распространение в качестве источников питания для бытовой техники, потребительской электроники, электроинструмента, электромобилей, электровелосипедов, скутеров и т. п. По сравнению с вышеописанными свинцово-кислотными и щелочными АКБ литий─ионные модели имеют более высокую энергоёмкость.

Происходящие процессы
В литиевый электрохимической системе сейчас используются различные химические соединения и периодически разрабатываются новые. Мы рассмотрим реакции, происходящие при заряде в большинстве распространённых коммерческих Li─Ion батареях.
Отрицательный электрод выполняется из материала, содержащего углерод. Благодаря его природе и составу электролита происходит процесс интеркаляции ионов лития в углерод. Углеродная матрица обладает слоистой структурой, которая может быть упорядоченной или частично упорядоченной. Это уже зависит от конкретного углеродосодержащего материала.
Материалы, используемые для производства положительного электрода, могут отличаться для различных разновидностей литиевых батарей. Чаще всего для этих целей используются литированные оксиды кобальта или никеля. Используются также литий─марганцевые шпинели.
При заряде литий─ионного аккумулятора на электродах протекают следующие реакции.
C + xLi + + xe — -> CLix
В процессе интеркаляция ионы лития из электролита внедряются между слоями углерода. При этом объём углеродной матрицы меняется незначительно. Этими качествами был обусловлен выбор углерода в качестве материала анода. Помимо материала, содержащего углерод, в отрицательном электроде могут быть такие добавки, как олово, серебро и их сплавы. В некоторых моделях встречаются композитные материалы.
Режимы заряда
Процесс заряда литий─ионных аккумуляторов комбинированный и проходит в два этапа. На первой стадии ведётся зарядка током, величина которого составляет от 20 до 100% от номинальной емкости батареи. Этот этап продолжается до того, пока напряжение АКБ не достигнет 4,1 вольта. После этого начинается второй этап, во время которого заряд ведётся при постоянном напряжении. По времени вся зарядка продолжается около 3 часов (при максимально допустимом токе), из которых на первый этап отводится один час. Более подробно о процессе заряда литиевых аккумуляторов можно прочитать в этой статье.
Окончание заряда фиксируется в тот момент, когда напряжение достигло максимального (4,1─4,2 В), а ток уменьшился до 3% от своей величины в начале процесса. В некоторых случаях возможен третий этап, который представляет собой хранение. Этот этап представляет собой периодическую подзарядку для компенсации ёмкости, потерянной в результате саморазряда.
Если увеличивать ток заряда выше 0,2─1*С, это не приводит к уменьшению времени процесса. В этом случае просто сокращается первый и увеличивается второй этап.
Бывают зарядные устройства, которые обеспечивают только первый этап зарядки. При таком варианте степень заряженности батареи составляет около 70─80%.
Вернуться к содержанию
Источник
Как предотвратить взрыв водорода в тяговом аккумуляторе
У взрыва аккумуляторов обидные причины — спешка, неаккуратность водителей, ошибки в обслуживании. При этом у свинцово-кислотных батарей есть одна особенность, которая повышает риск взрыва — это выделение водорода при зарядке. О тонкостях работы с такими аккумуляторами рассказывает Александр Логинов, генеральный директор компании «Энергоэлемент», которая продает и обслуживает все типы тяговых аккумуляторов.
Водород настолько взрывоопасен, что при концентрации в воздухе более 4% способен сдетонировать без внешнего воздействия, сам по себе. Столько водорода накопится за 2 часа, если мы возьмем пять самых ходовых батарей 48 В 500 А·ч и поставим заряжаться без вентиляции в типовой зарядной комнате. Но на деле такой концентрации не потребуется: достаточно тонкой струйки газа и искры — и аккумулятор рванет.
Почему образуется водород
Выделение водорода в свинцово-кислотных аккумуляторах — естественный процесс. Однако при ошибках в обслуживании этот газ образуется сверх меры. Чтобы разобраться, что это за ошибки, рассмотрим сначала, откуда вообще берется водород в батарее.
Зарядка аккумулятора проходит в три фазы. Первая — основной заряд, вторая — дозаряд и третья — перемешивающий или уравнительный заряд.
В первой фазе батарея принимает ток высокой мощности, а напряжение постепенно растет. Вся энергия поступает в пластины электродов и идет на восстановление свинца.
Вторая фаза начинается, когда напряжение достигло нужного уровня. Далее оно остается постоянным, а ток падает, пока батарея не зарядится до 100%. Сколько бы тока мы ни вливали после этого, пластины уже не смогут его принять.
Излишек тока будет уходить в воду и запустит ее электролиз — вода начнет разлагаться на молекулы кислорода и водорода. Аккумулятор «закипит» и будет выделять огромное количество энергии. Это и есть третья фаза.
Считается, что такого кипения нужно избегать. На деле не совсем так. Непродолжительное кипение аккумулятора необходимо: пузырьки газа поднимаются вверх и перемешивают разные по плотности слои электролита, чтобы выровнять. А вот затягивать кипение нежелательно.
Что усиливает выделение водорода
Зарядка трансформаторными устройствами с профилем WoWa. У зарядных устройств есть коэффициент перезаряда — он показывает, какой излишек энергии идет на третью фазу. Современные высокочастотные устройства подают разный ток в зависимости от фазы, а их коэффициент перезаряда равен 1,03—1,07. В отличие от них трансформаторные зарядные устройства WoWa подают ток постоянной мощности. Коэффициент перезаряда таких устройств составляет 1,2, то есть третья фаза начинается раньше, а водорода выделяется больше.
Зарядка горячей батареи также приводит к раннему началу третьей фазы. Чем выше температура, тем ниже напряжение, при котором начинается электролиз воды. Фактически из-за этого в не успевшей остыть батарее третья фаза начнется одновременно с первой. Батарея критически нагревается — до 90 градусов, это ведет к коррозии электродов и перерасходу воды. Если после заряда открыть крышку для долива воды, капли горячего электролита полетят наружу.
Зарядка аккумулятора без одного из элементов. Зарядное устройство подает ток высокой мощности, пока не получит нужное напряжение. Так как прибор заряжает не отдельные аккумуляторные элементы, а батарею в целом, нужное напряжение равно сумме напряжения всех элементов. Это число записано в профиле зарядного устройства, и прибор не может сделать перерасчет, если какого-то элемента нет. В итоге оставшиеся элементы получают перенапряжение, а избыток энергии идет в электролиз воды.
Работа на старых аккумуляторах более одного разряда в день. На новом аккумуляторе литр воды испаряется за пять-семь циклов работы, а на старых — за один-два. Чем ниже уровень электролита, тем больше внутри элемента пространства для скапливания водорода. Это особенно опасно для техники с высокими аккумуляторами, например, узкопроходных высотных штабелеров.
Как происходит взрыв
В крышках для долива воды в аккумулятор есть отверстия диаметром 2 мм — через них водород выходит их элемента. Это удобнее, чем каждый раз открывать крышку с риском выплеснуть кислоту на корпус.
После зарядки водород еще какое-то время выходит наружу и скапливается в пазухах крышек. Если не дождаться полного выветривания, газ может взорваться. К взрыву приводят искры, сильный нагрев, открытое пламя, а также короткое замыкание — из-за коррозии перемычек, оголенных проводов, трещин в пластиковой обшивке.
Чаще всего изоляция разрушается, когда водители торопятся приступить к погрузке и забывают об аккуратном обращении. Например, тянут силовой кабель не за коннектор, а за провод, из-за чего место соединения оголяется. В спешке забывают поправить провода и придавливают их батареей или сидушкой — пара таких ударов и изоляция лопается.
Мы занимаемся обслуживанием аккумуляторов и не раз сталкивались с последствиями взрыва водорода. Вот некоторые случаи из нашей практики.
Пример 1. У узкопроходных высотных штабелеров и погрузчиков с грузоподъемностью от двух тонн через аккумулятор идет ток мощностью 1000 А·ч. Опасность в том, что он может раскалить всю проводку батареи. К тому же у такой техники высокие аккумуляторы и места для скопления водорода много.
В этом примере у штабелера из-за коррозии перегревалась одна из перемычек батареи. Водитель не выждал паузу и начал работу, когда концентрация водорода под крышкой была максимальной. Перемычка перегрелась и водород сдетонировал. Взорвался один элемент. На поставку нового из Европы ушло четыре недели — все это время батарея простаивала.
Пример 2. К замыканию привело использование неизолированной траверсы для подъема аккумулятора. Когда изоляция изнашивается со временем, возрастает риск попасть деталями траверсы на оголенные элементы «+» и «−» батареи, например, в этом случае — на поврежденные болты.
Пример 3. Когда водители ставят аккумулятор в технику, то в спешке забывают о мерах безопасности. Складская техника массивная, а места для батареи впритык — можно пережать провода.
При установке аккумулятора в электропогрузчик водитель не рассчитал высоту подъема и угол наклона тележки. Провода прижало к корпусу и взорвалось 12 элементов. Куски пластика с кислотой разлетелись вокруг и только случайно не попали в водителя.
Пример 4. Водитель ричтрака не поправил силовой кабель, когда задвигал аккумулятор. Провода попали между ним и бортом ричтрака, и их срезало. Произошло короткое замыкание и 6 элементов взорвались. Ситуацию усугубило то, что батарею почти не обслуживали, уровень электролита был низкий, а места для водорода много.
Пример 5. Во время заряда аккумулятор находился в тягаче и был закрыт сидушкой с герметичной крышкой — инженер забыл ее поднять. Водород накапливался под крышкой, да еще сверх меры, потому что батарею заряжали без одного элемент. Взрыв произошел прямо под водителем, когда он включил зажигание. Парень получил контузию, из ушей пошла кровь. К работе он смог вернуться только через две недели. А аккумулятор стоимостью 11 тысяч евро вышел из строя.
Иногда к взрыву приводит халатность механиков, например, когда начинают чистить клеммы, не отключив батарею от зарядного устройства. Такая забывчивость — все равно что уехать с заправки, не вынув пистолет из бака.
При работе со свинцово-кислотными батареями важно соблюдать требования ГОСТа по утилизации водорода из зарядной комнаты. Как правило, к недостаточной вентиляции приводит плохая вытяжка или одновременная зарядка слишком многих аккумуляторов. Однако вместо того, чтобы устранить нарушения, компании порой предпочитают откупиться от пожарного надзора.
Мы рекомендуем установить в зарядной комнате датчик водорода, следить за состоянием изоляции всех элементов батареи и делать паузу в 15 минут после заряда. Надеемся, наш опыт поможет компаниям предотвратить чрезвычайные ситуации.
Источник



