- Как устроен Li-Ion аккумулятор?
- Как устроена литий-ионная батарея?
- Типы Li-ionаккумуляторов
- Как работает литиевый аккумулятор?
- Особенности зарядкиLi-ionэлементов
- Защита литиевых аккумуляторов
- Производство литиевых элементов питания
- Литий-ионный аккумулятор (Li-ion)
- Принцип работы литий-ионного аккумулятора
- Строение литий-ионного аккумулятора
- Процесс заряда и разряда литий-ионного аккумулятора
- Слой разделителя в литий-ионном аккумуляторе
- Из чего делают литий-ионный аккумулятор
- Литий-ионные аккумуляторы в автомобиле Tesla
- Защитный SEI-слой
- Заключение
Как устроен Li-Ion аккумулятор?
Автономную работу всевозможных устройств,отмобильных гаджетов до персонального электротранспорта, обеспечивают аккумуляторы. С учетом необходимых значений емкости и напряжения, они объединяются в аккумуляторные батареи. Ключевые характеристики АКБ – емкость, напряжение, масса, время восполнения заряда, допустимый температурный режим – зависят от типа используемой химии.
Для автономного питания современной техники успешно используются литий-ионные аккумуляторы. Они имеют большой циклический ресурс, малый саморазряд, широкий температурный диапазон и солидную удельную емкость. Катод у таких элементов выполнен из производных лития, а заряд переносят ионы Li. Далее мы подробнее рассмотрим устройство Li-ion аккумуляторов и принцип их работы.
Как устроена литий-ионная батарея?
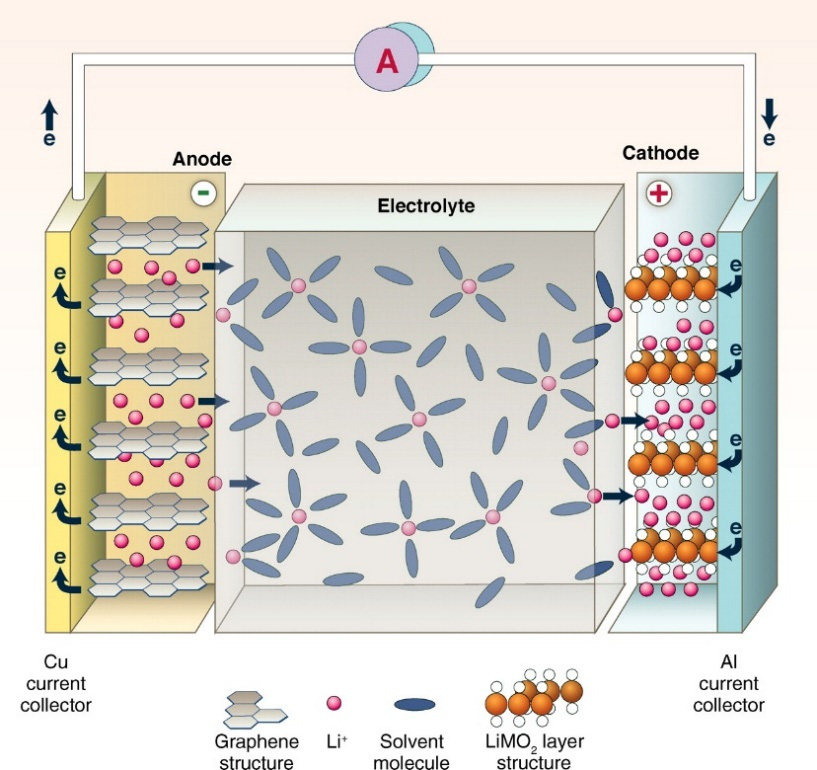
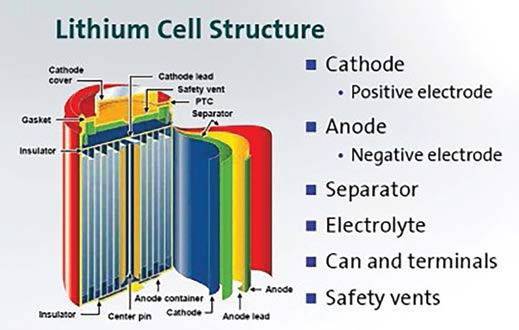
В основе конструкции литий-ионного аккумулятора– 2 составляющие: анод, выполненный из пористого углерода на фольге из меди, и катод – из оксида лития на фольге из алюминия. Их разделяет пористый сепаратор из полипропилена, обильно пропитанный электролитом, который выполняет функции проводника. Система находится в герметичном корпусе. Электроды подключены к токосъемникам. Некоторые аккумуляторы дополнительно имеют клапан-предохранитель для сброса внутреннего давления.
Пластины из меди и алюминия, смазанные электролитом и разделенные пористой прослойкой, обычно сворачиваются в рулон. В итоге получается элемент цилиндрической формы. При другом способе укладки пластин получаются изделия в форме призм и пакетов. Состав катода бывает разным: LiMn2O4, LiFePO4, LiCoO2,LiMnO2, LiMnRON, LiC6, LiNiO2и т.д.
Типы Li-ionаккумуляторов
В зависимости от используемого материала катода литиевые элементы бывают:
- Литий-марганцевые (LiMn2O4, LNO). Имеют меньшее внутреннее сопротивление, высокую мощность и умеренную емкость – 100–150 Вт·ч/кг. Стандартные токи заряда и разряда – до 1С, но есть модели с С-рейтингом зарядки до 3С и С-рейтингом разряда до 10С, а в импульсном режиме – до 50С. Ресурс – около 500 циклов. Применяются такие накопители в электроинструменте, силовых агрегатах, медицинском оборудовании.
- Литий-кобальтовые (LiCoO2, LCO). Имеют высокую энергоемкость (150–200 Вт·ч/кг), но уступают аналогам по термической стабильности и сроку службы (500–1000 циклов). Токи заряда и разряда для таких элементов не должны превышать 1С. Накопители энергии на основе кобальта встречаются все реже, но еще используются в мобильных телефонах, цифровых камерах, ноутбуках.
- Литий-никель-марганец-кобальт-оксидные (NMC, NCM). Обеспечивают высокую мощность и емкость – 150–220 Вт·ч/кг, выдерживают 1000–2000 циклов. Стандартные токи заряда и разряда – 1С. Используются в медицинском и промышленном оборудовании, электровелосипедах и других видах электротранспорта.
- Литий-никель-кобальт-алюминий-оксидные (NCA). Отличаются высокой удельной энергоемкостью – 200–260 Вт·ч/кг. Имеют ресурс около 500 циклов, зарядные токи 0,7С и разрядные 1С. Обеспечивают автономное питание промышленного и медицинского оборудования, электрических силовых агрегатов и других устройств, требующих высокой емкости.
- Литий-железо-фосфатные (LFP, LiFePO4). Отличаются большим ресурсом (более 2000 циклов), термической и химической стабильностью, высокой безопасностью эксплуатации и малым внутренним сопротивлением. Их удельная энергоемкость составляет 90–120 Вт·ч/кг, ток зарядки – 1С, ток разрядки – до 25С. Используются такие элементы питания в устройствах, для которых важна выносливость аккумов, способность работать на морозе и выдерживать высокие токи нагрузки.
- Литий-титанатные (LiTi). Отличаются низким номинальным напряжением (2,4 В) и удельной энергоемкостью 70–80 Вт·ч/кг, но быстро заряжаются, имеют широкий температурный диапазон и ресурс 3000–7000 циклов. Номинальные токи зарядки 1С, максимум – 5С. Допустимые разрядные токи – 10С, а при импульсной подзарядке – 30С. Литий-титанатные элементы считаются самыми безопасными. Используются они в уличном освещении, ИБП, электротранспорте.
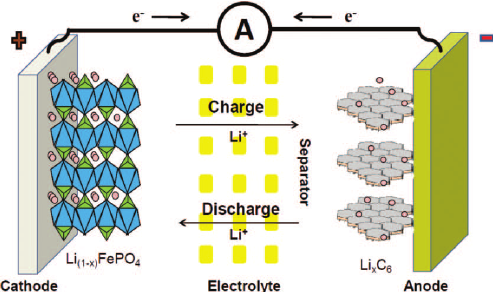
Как работает литиевый аккумулятор?
Принцип работы Li-ion аккумуляторов идентичен для элементов всех типов, независимо от материала катода.Когда на электроды подается напряжение – «плюс» на оксид лития и «минус» на графит – положительно заряженные ионы лития отцепляются от молекул оксида и переходят на углеродную пластинку. В результате протекает окислительная реакция, и аккумулятор заряжается.
При работе литиевого аккумулятора под нагрузкой протекает обратный процесс. Ионы Li + возвращаются на пластинку из оксида лития, в свое стандартное состояние. Графитовая пластинка на фольге из меди становится «минусом», а оксид лития на фольге из алюминия – «плюсом».
Особенности зарядкиLi-ionэлементов
Литий-ионные элементы питания чувствительны к перезаряду. На поверхности анода при чрезмерном заряде осаждается металлический литий. Он выглядит как мелкий мшистый осадок и способен вступать в реакцию с электролитом. На катоде при перезаряде активно выделяется кислород. Внешне это может проявляться в виде интенсивного нагрева, роста давления и разгерметизации элемента.
Заряжаются Li-ionаккумуляторы в 2 этапа:
- При стабильном значении тока 0,2С–1С до рекомендованного производителем напряжения, обычно – 4,1–4,2 В. Длится эта стадия около 40 минут.
- При неизменном напряжении. Процесс зарядки завершается, когда значение зарядного тока уменьшается до величины, составляющей 3% от начального значения.
Быстрее происходит зарядка в импульсном режиме.Но для продления срока службы литиевых элементов их рекомендуется заряжать током, номинал которого составляет 50% от значения емкости, т.е. 0,5С.
Защита литиевых аккумуляторов
Элементы питания на основе лития защищены от коротких замыканийвнутри системы, например, с помощью 2-слойного сепаратора. Один из его слоев выполняется не из полипропилена, а из аналога полиэтилена. При риске короткого замыкания, к примеру, если дендриты лития прорастают к катоду, защитный слой локально нагревается, частично плавится, становится непроницаемым и блокирует последующее прорастание дендритов.
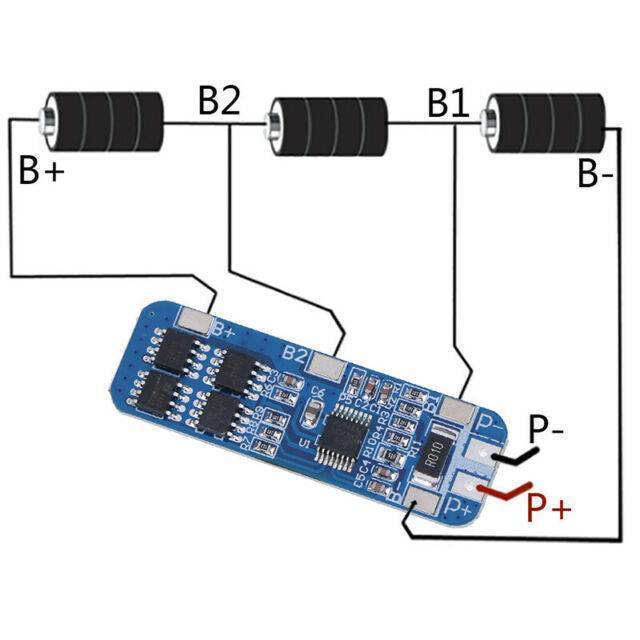
Для защиты от избыточного заряда и глубокого разряда накопители энергии снабжаются специальными ограничителями – платами защиты по току и напряжению. Они не допускают выхода напряжения за границы рекомендованного диапазона и в критических ситуациях автоматически отключают элемент от питания или нагрузки.
Поэтому для безопасной работы элементов и аккумуляторных батарей важно использовать BMSплаты. В противном случае высок риск повреждения аккумуляторов и их преждевременного выхода из строя. Такой контроллер зарядно-разрядного процесса может устанавливаться и на отдельные аккумуляторы, и на собранную из них батарею.
Производство литиевых элементов питания
Сырье для основных элементов в схеме Li-ion аккумуляторов – катода и анода – имеет вид мелкофракционного черного порошка. Чем мельче частицы, тем больше получается эффективная площадь электродов. Оптимальная форма частиц – сферическая, с гладкими краями, т.к. неровности чувствительны к токовым нагрузкам.
Производственный процесс состоит из следующих этапов:
- Порошковидные материалы наносятся в виде суспензии на фольгу. Аноды и катоды обычно производятся в различных цехах, чтобы обеспечить максимальную чистоту материалов. Металлическая фольга играет роль токоприемника.
- Фольга с нанесенными материалами сушится, разделяется на полоски и складывается в несколько слоев. Процесс сворачивания строго контролируется, т.к. любые дефекты способны привести к коротким замыканиям внутри системы.
- Между пластинами анода и катода зажимается сепаратор, обработанный электролитом.
- Пластинки сворачиваются рулоном или по другой схеме и помещаются в корпус.
Готовые изделия проходят тестирование – контролируемый цикл заряда-разряда. Подзарядку начинают с минимального напряжения и с постепенным его повышением.Протестированные изделия заряжаются до оптимального уровня, чтобы исключить риск значительного падения напряжения из-за саморазряда, и поставляются в продажу.
Предыдущая статья нашего блога посвящена сигнализации для электровелосипедов.
Источник
Литий-ионный аккумулятор (Li-ion)
В настоящее время литий-ионный аккумулятор используется абсолютно во всей домашней и портативной электронике.

Можно без преувеличения сказать: без портативных источников питания, мир современной техники был бы намного беднее. Все разнообразие карманных электронных гаджетов, приборов, смартфонов, гироскутеров, электромобилей наконец, стало возможным благодаря литий-ионным аккумуляторам.
Принцип работы литий-ионного аккумулятора
Давайте рассмотрим литий-ионный аккумулятор. Как видите, он состоит из нескольких слоев с различным химическим составом.

В основе работы литий-ионного аккумулятора лежит, так называемый, электрохимический потенциал. Суть его в том, что металлы стремятся «отдавать» свои электроны. Как видно на рисунке ниже, наибольшая способность к отдаче электронов – у лития, а наименьшая – у фтора. Если такой атом отдает свой электрон, то он становится положительным ионом.
Первая в истории электрическая батарейка, созданная более 200 лет назад Алессандро Вольтой, работала как раз на принципе электрохимического потенциала. Вольта взял два металла с разными электрохимическими потенциалами (цинк и серебро) и получил электрический ток. В честь его открытия такую “батарейку” назвали Вольтовым столбом.

В 1991 г. Sony выпустила первый коммерчески успешный литий-ионный аккумулятор.
В литий-ионных элементах используется металл с наибольшей способностью отдавать электроны – литий. У лития всего один электрон на внешней орбите, и он постоянно стремится его «потерять».

Из-за этого литий считается чрезвычайно химически активным металлом. Он реагирует даже с водой и воздухом. Но активен только чистый литий, а вот его оксид, напротив, очень стабилен.

Это свойство лития как раз используется при создании литий-ионных аккумуляторов.
Допустим, мы каким-то образом отделили атом лития от оксида. Этот атом будет крайне нестабилен и сразу превратится в положительный ион, потеряв электрон.

Однако в составе оксида литий гораздо более стабилен, чем одинокий атом лития. Если мы сможем каким-то образом обеспечить движение по двум отдельным путям для электрона и для положительного иона лития, то ион самостоятельно достигнет оксида и встанет там на свое место. При этом мы получим электрический ток благодаря движению электрона.

Итак, можно получить электрический ток из оксида лития, если сначала отделить атомы лития от оксида и затем направить потерянные ими электроны по внешней цепи. Рассмотрим, как эти две задачи решаются в литий-ионных элементах.
Строение литий-ионного аккумулятора
Помимо оксида лития, элементы содержат также электролит и графит. В графите связь между слоями гораздо слабее, чем между атомами внутри слоев, поэтому графит имеет слоистую структуру.

Электролит, помещенный между оксидом лития и графитом, служит барьером, пропускающим сквозь себя только ионы лития. Электроны же не могут проникать сквозь электролит и отскакивают от него, как теннисный мячик об стенку. В качестве электролита используется органическая соль лития, которая наносится на слой разделителя (о разделителе ниже в статье).

Процесс заряда и разряда литий-ионного аккумулятора
Итак, у нас есть разряженный аккумулятор

Давайте же его зарядим. Для этого нам нужен какой-либо источник питания. Что произойдет в этот момент на самом литий-ионном аккумуляторе? Положительный полюс начнет притягивать электроны, «вытаскивая» их из оксида лития.

Поскольку электроны не могут проникать через электролит, то они движутся по внешней цепи через источник питания.

и в конце концов достигают графита

где очень удобно располагаются в слоях графита.

В этот же самый момент положительные ионы лития притягиваются отрицательным полюсом, проходя сквозь электролит и также попадают в графит, размещаясь между его слоями.

Когда все ионы лития достигнут графита и будут «захвачены» его слоями, батарея будет полностью заряжена.

Такое состояние батареи неустойчивое. Это можно представить как шар, который находится на самой верхушке холма и в любой момент может скатиться.

Вот мы и достигли первой цели: электроны и ионы лития отделены от оксида. Теперь надо как-то сделать так, чтобы электроны и ионы двигались разными путями. Как только мы подключим какую-либо нагрузку к нашему заряженному литий-ионному аккумулятору, то начнется обратный процесс. В этом случае ионы лития через электролит пожелают вернуться в свое изначальное состояние.

Поэтому они начнут двигаться обратно сквозь электролит, а электроны побегут через внешнюю цепь, то есть через нагрузку.

Так как электрический ток – это не что иное, как упорядоченное движение заряженных частиц, то в цепи лампочки накаливания возникнет электрический ток, который заставит эту самую лампочку светиться.

Как только все электроны “убегут” из графита, то батарея полностью разрядится. Чтобы ее снова зарядить, достаточно поставить аккумулятор “на зарядку”.

При этом графит сам по себе не участвует в химических реакциях – он лишь служит «складом» для ионов и электронов лития.
Слой разделителя в литий-ионном аккумуляторе
Если внутренняя температура элемента по какой-то причине начнет расти, жидкий электролит высохнет, и произойдет короткое замыкание между анодом и катодом. В результате элемент может загореться или даже взорваться.

Чтобы этого не произошло, между электродами помещается дополнительный изолирующий слой, называемый разделителем. Разделитель проницаем для ионов лития благодаря наличию микропор. Электроны он не пропускает.

Из чего делают литий-ионный аккумулятор
В реальных литий-ионных аккумуляторах графит и оксид лития наносятся в виде покрытия на медную и алюминиевую фольгу. Ниже на рисунке мы видим, что на тонком листе меди у нас располагается графит, а на тонком листе алюминия – оксид лития.

Минус аккумулятора снимается с медной фольги, а плюс – с алюминиевой.

ну а между ними располагается еще разделитель, пропитанный электролитом

Для того, чтобы уменьшить объем, все эти три слоя сворачивают в “рулончик”.


образуя при этом всем нам знакомую литий-ионную цилиндрическую батарейку

Литий-ионные аккумуляторы в автомобиле Tesla
Вообразите мир, в котором все машины оснащены электродвигателями, а не двигателями внутреннего сгорания. Электромоторы превосходят ДВС практически по всем техническим показателям, да к тому же намного дешевле и надежнее. У ДВС есть существенный недостаток: он выдает достаточный крутящий момент лишь в узком диапазоне скоростей. В общем, электродвигатель – однозначно лучший выбор для автомобиля. Об этом мы писали еще в статье про автомобиль Тесла.

Но есть одно «узкое место», из-за которого электрическая революция в автопроме постоянно откладывается – это источники питания. Долгое время громоздкие, тяжелые, недолговечные и ненадежные аккумуляторы электромобилей никак не могли составить конкуренцию полному баку бензина. Но все изменилось, когда на рынок вышел производитель электромобилей Тесла.
Именно литий-ионные аккумуляторы использует компания Тесла для своих электрокаров.

Стандартный элемент выдает напряжение 3,7 – 4,2 В. Множество таких элементов, соединенных последовательно и параллельно, образуют модуль.

Литий-ионные элементы при работе выделяют много тепла. При этом высокая температура снижает срок службы и эффективность самих элементов. Для контроля температуры, а также их уровня заряда, защиты от перезаряда и общего состояния элементов питания, служит специальная система управления батареями (Battery management system, сокращенно BMS). В батареях Tesla используется спиртовая система охлаждения. BMS регулирует скорость движения спирта в системе, поддерживая оптимальную температуру батарей.

Еще одна важнейшая функция BMS – защита от перезаряда. Допустим, есть три элемента с разной емкостью. Во время зарядки элемент с большей емкостью зарядится сильнее двух остальных. Чтобы этого не допустить, BMS использует так называемое выравнивание заряда элементов (cell balancing). При этом все элементы заряжаются и разряжаются равномерно и защищены от чрезмерного или недостаточного заряда.
И в этом преимущество Tesla над технологией аккумуляторов Nissan. У Nissan Leaf серьезная проблема с охлаждением аккумулятора из-за большого размера элементов и отсутствия системы активного охлаждения.

У конструкции с множеством маленьких цилиндрических элементов есть и еще одно преимущество: при большом расходе энергии нагрузка распределяется равномерно между всеми элементами. Если бы вместо множества маленьких элементов был один огромный элемент, из-за постоянных нагрузок он очень быстро бы пришел в негодность. Tesla сделала ставку на маленькие цилиндрические элементы, технология производства которых уже хорошо отработана. Более подробно про батарейный модуль Тесла читайте в этой статье.
Защитный SEI-слой
Во время первой зарядки внутри литий-ионного элемента происходит одно замечательное явление, спасающее элемент от скорой «смерти». Неожиданной проблемой оказались электроны, находящиеся в слое графита. При контакте с электролитом они начинают разрушать его. Но одно случайное открытие позволило не допустить контакт электронов с электролитом. При первой зарядке элемента, как мы уже говорили, ионы лития движутся сквозь электролит. В процессе этого движения молекулы растворенного в электролите вещества покрывают ионы. Достигнув графитового слоя, ионы лития вместе с молекулами раствора электролита реагируют с графитом, образуя так называемая промежуточную фаза твердого электролита (solid electrolyte interphase, или SEI-слой). Этот слой предотвращает контакт электронов с электролитом, предохраняя электролит от разрушения.

Вот так проблема случайным образом решилась сама собой. Хотя эффект SEI был открыт случайно, в последующие два десятилетия ученые целенаправленно улучшали процесс, подбирая наиболее эффективную толщину и химический состав.
Заключение
Сегодня уже удивительно, что еще два десятка лет назад в электронных гаджетах не применялись литий-ионные аккумуляторы. Индустрия литий-ионных аккумуляторов развивается с фантастической скоростью: ожидается, что в ближайшие несколько лет их рынок достигнет 90 млрд. долларов. Современные литий-ионные батареи способны выдержать примерно 3000 циклов зарядки-разрядки – это уже приличный показатель, но еще есть, куда расти. Лучшие умы во всем мире трудятся над тем, чтобы повысить их долговечность до 10 000 циклов. В этом случае аккумулятор электромобиля не придется заменять целых 25 лет. Миллионы долларов вкладываются в исследования, которые позволят заменить графит на кремний в качестве «хранилища» в литий-ионных элементах. Если это удастся сделать, их емкость возрастет более чем в пять раз! В настоящее время мир переходит уже на литий-полимерные аккумуляторы, которые показали себя чуточку лучше, чем литий-ионные.
Источник