- Сепаратор для литий ионный аккумулятор
- Сепараторы аккумуляторных батарей
- Какую функцию выполняет в электрической батарее сепаратор?
- Сепаратор как предохранитель в литий-ионном аккумуляторе
- Как создают аккумуляторные батареи
- Li-ion — литий-ионные
- Li-po — литий-полимерные
- Li-po и технологии
- Li-po vs Li-ion
- Литий
- Извлечение лития
- Другие химические элементы
- Процесс производства батареи
Сепаратор для литий ионный аккумулятор
Сепараторы аккумуляторных батарей
11.02.09 | Рубрика: Свинцово-кислотные АКБ. Просмотры: 17 058
В настоящее время на мировом рынке представлено несколько видов аккумуляторных батарей, различное устройство которых предъявляет обособленные требования к сепараторам. Тип химии аккумулятора определяет все его основные характеристики, достоинства и недостатки. Невозможно выделить «лучший» тип аккумулятора. Каждому из них свойственны свои плюсы и минусы, которые делают аккумулятор оптимальным для одних применений и совершенно неприемлемым для других.
В современной технике используются пять основных типов аккумуляторов, отличающихся по своему химическому составу:
1. Никель-кадмиевые (NiCd). Хорошо отработанная и изученная технология, но обладает низкой плотностью энергии. Используется там, где важны долговечность, способность обеспечить высокий ток нагрузки и малая стоимость. Основные области применения: портативные радиостанции, медицинское оборудование, профессиональные видеокамеры и электроинструмент. NiCd аккумуляторы содержат токсичные материалы и являются экологически грязными.
2. Никель-металлогидридные (NiMH). По сравнению с NiCd имеют более высокую плотность энергии, но меньшее время жизни. NiMH не содержат токсичных материалов. Применяются в мобильных телефонах и портативных компьютерах.
3. Литий-ионные (Li-ion). Наиболее бурно развивающаяся технология. Используются там, где нужна высокая плотность энергии и малый вес. Li-ion дороже всех других аккумуляторов. При эксплуатации необходимо строго соблюдать режимы заряда и разряда, указанные производителем из соображений безопасности. Применяются в компьютерах и сотовых телефонах.
4. Литий-полимерные (Li-polymer). Задуманы как удешевленная версия Li-ion аккумуляторов. Этот тип химии по плотности энергии аналогичен Li-ion . Это позволяет делать Li-polymer аккумуляторы очень компактными. В основном, используются в мобильных телефонах.
5. Свинцово-кислотные аккумуляторы (LA). Применяются там, где требуется большая мощность, а вес не имеет значения. Наиболее распространенный тип аккумулятора в мире (из расчета ампер-часов). Основная область применения — стартерные батареи. Герметичные свинцово-кислотные (SLA) — один из видов свинцово-кислотных аккумуляторов. Применяются там, где требуется большая мощность, а вес не имеет значения. Типовые области применения — стационарное медицинское оборудование, электромобили, системы аварийного энергоснабжения, UPS (источники бесперебойного питания).
6. Алкалиновые аккумуляторы — созданы для замены бытовых батареек. Хорошо подходят в случаях, когда не требуется большой мощности. Небольшое время жизни этих аккумуляторов компенсируется очень низким током саморазряда, что делает их оптимальными для применения в портативных магнитолах и фонарях.
Ниже приведена сводная таблица параметров наиболее популярных аккумуляторов.
Технологические характеристики аккумуляторных батарей
Источник
Какую функцию выполняет в электрической батарее сепаратор?
Главные составляющие части электрической батареи — анод и катод, и эти два электрода изолированы друг от друга сепаратором. Сепаратор, пропитанный электролитом, образует катализатор, который способствует движению ионов от катода к аноду при заряде, и в обратном направлении при разряде. Ионы представляют собой атомы, которые получили или потеряли электроны, и благодаря этому перестали быть электрически нейтральными. Несмотря на то, что ионы свободно перемещаются между электродами, сепаратор является изолятором, то есть не имеет электрической проводимости.
Небольшое количество тока, которое может проходить через сепаратор, формирует явление саморазряда, которое присутствует во всех электрических батареях в той или иной степени. Саморазряд в конечном итоге истощает заряд батареи при длительном хранении. На рисунке 1 показано строение литий-ионного элемента с сепаратором и поток ионов между электродами.
Рисунок 1: Ионный поток через сепаратор литий-ионного элемента. Сепаратор формирует барьер между анодом и катодом при одновременном обеспечении обмена ионов лития с одной стороны на другую.
Ранние модели электрических батарей были затопленные, в том числе, свинцово-кислотные и никель-кадмиевые. С изобретением герметичных никель-кадмиевых в 1947 году и необслуживаемых свинцово-кислотных в 1970-х, электролит стал впитываться в пористый сепаратор, который плотно располагался между электродами для лучшего обеспечения химических реакций. Конструктивно сепаратор и электроды в таких батареях образовывают прочный твердый механический узел, который имеет характеристики, аналогичные затопленным моделям, но меньше по размерам и может быть установлен в любом положении без риска утечки электролита. Газы, вырабатываемые во время зарядки, рекомбинируют обратно в воду, следовательно, такие аккумуляторы не требуют дополнительного обслуживания.
| Standard Range AGM | Deep Cycle Range AGM | Gellyte Range GEL |
 |  |  |
| 10 — 12 лет / 600 циклов | 10 — 12 лет / 700 циклов | 10 — 12 лет / 750 циклов |
| универсальная серия AGM | для глубоких разрядов AGM | универсальная серия GEL |
Первые сепараторы делались из каучука, стекловолокна, целлюлозы и полиэтилена. Использовалось даже дерево, но оно быстро теряло свои свойства из-за электролита. В никелевых батареях используют сепараторы из пористой полиолефиновой пленки, нейлона или целлофана. В герметичных свинцово-кислотных AGM [BU-201a] аккумуляторах в качестве сепаратора используется стекловолокно, смоченное серной кислотой.
Ранние модели гелевых свинцово-кислотных аккумуляторов, разработанные в 1970-х, преобразовывали жидкий электролит в гелеобразную пасту путем смешивания серной кислоты и содержащего кремний агента. Гелевые и AGM аккумуляторы имеют небольшие различия в производительности; гелевые широко используются в ИБП, а AGM — в роли стартерных и глубокоразрядных аккумуляторов. (Смотрите также BU-201: Как устроена свинцово-кислотная батарея).
Потребительские литий-ионный батареи используют полиолефин в качестве сепаратора. Этот материал обладает отличными механическими свойствами, хорошей химической стабильностью и низкой стоимостью. Полиолефины — класс высокомолекулярных соединений (полимеров), получаемых из низкомолекулярных веществ — олефинов (мономеров). Полиолефины вырабатываются из нефти или природного газа путём полимеризации одинаковых (гомополимеризации) или разных (сополимеризации) мономеров в присутствии катализатора.
Сепаратор для литий-ионного аккумулятора должен быть проницаемым и иметь поры размером от 30 до 100 нм. (Нм означает нанометр, который является одной миллионной миллиметра, что соответствует размеру 10 атомов). Рекомендуемая пористость составляет 30-50 процентов. Такой показатель обеспечит достаточное количество жидкого электролита и позволит перекрывать поры при перегреве аккумулятора.
Сепаратор как предохранитель в литий-ионном аккумуляторе
При высоких температурах происходит остановка работы литий-ионного аккумулятора путем перекрытия пор в сепараторе из-за его плавления. Полиэтиленовый сепаратор начинает плавиться при 130°С. Это останавливает транспорт ионов, эффективно “выключая” аккумулятор. Без этого свойства сепаратора значение температуры может повышаться и далее, достигнув значения теплового пробоя, что чревато возгоранием или даже взрывом. Присутствие такого механизма предохранения помогает литий-ионным аккумуляторам проходить различные тесты безопасности, которые включают в себя имитацию высоты, тепловое воздействие, вибрации, удары, внешнее короткое замыкание, перезарядку и принудительный разряд. (Смотрите также BU-304a: Проблемы безопасности литий-ионных аккумуляторов).
| Trojan Marine RV | AGM Deep Cycle | Trojan GEL Deep Cycle |
 |  |  |
| 10 — 12 лет / 700 циклов | 10 — 12 лет / 600 циклов | 10 — 12 лет / 800 циклов |
| для речного и морского траспорта | для электромоторов, солнечных электростанций, высоких нагрузок | |
Большинство потребительских аккумуляторов для мобильных телефонов, планшетов и прочих устройств имеют однослойный полиэтиленовый сепаратор. Более же крупные промышленные образцы имеют уже трехслойный сепаратор, который обеспечивает повышенную защиту в многоэлементных системах при экстремальных температурах. На рисунке 2 показан трехслойный сепаратор ПП/ПЭ/ПП, состоящий из полиэтилена, зажатого полипропиленовыми слоями. В то время как внутренний полиэтиленовый слой начинает плавиться при 130°С, закрывая поры, внешние слои полипропилена сохраняют проводимость ионов до температуры в 155°С.
Рисунок 2: Вид сбоку на трехслойный ПП/ПЭ/ПП сепаратор. Комбинация материалов сепаратора с различными температурами плавления позволяет создать конструкцию с повышенной безопасностью. Полиэтилен плавится раньше полипропилена, чтобы закрыть поры и остановить движение электрического тока.
Дальнейшее улучшение сепаратора было сделано путем добавления керамического покрытия. Керамические частицы не плавятся, и их добавление обеспечивает дополнительный уровень безопасности. Керамическое покрытие используется в литий-кобальт-оксидных (LCO) аккумуляторах, в которых номинальное напряжение составляет 4,40 В на элемент вместо традиционных 4,20 В. Такое покрытие работает в тандеме со слоями полиэтилена и полипропилена и помещается рядом с положительной стороной для предотвращения электрического контакта.
Сепаратор должен быть как можно тоньше, обеспечивать достаточную прочность на разрыв и иметь хорошую стабильность конструкции на протяжении всей жизни аккумулятора. Поры должны быть равномерно распределены по всему сепаратору, и кроме того, материал сепаратора должен быть совместим с электролитом и позволять легко ему впитываться. Сухие участки сепаратора могут привести к увеличению температуры из-за повышенного сопротивления, что в конечном итоге может привести к выходу из строя такого элемента.
Существует общая тенденция к уменьшению толщины сепараторов. Толщина в 25,4 микрометра уже является стандартной, и проводятся разработки, которые способны уменьшить ее до 20, 16 и даже 12 микрометров без существенного ухудшения свойств элемента. (Один микрометр, также известный как микрон, составляет одну миллионную часть метра). Сепаратор с электролитом в современных литий-ионных элементах составляет лишь 3 процента от всего содержимого.
| Marin GEL Range | Deep Cycle GEL Range | Solar GEL Range |
 |  |  |
| 10 — 12 лет / 800 циклов | 10 — 12 лет / 800 циклов | 10 — 12 лет / 800 циклов |
| для электромоторов лодок и катеров | для глубоких циклических разрядов | для солнечных электростанций |
Но использование ультратонких сепараторов также поднимает и вопросы безопасности. Корпорации Sony пришлось отозвать 6 миллионов аккумуляторов из-за нескольких случаев возгорания. Причиной этих возгораний служили микроскопические частицы металла, которые вступали в контакт с частями батареи и приводили к короткому замыканию. Электрические элементы аккумуляторов Sony, о которых идет речь, имели толщину сепараторов между 20 и 25 мкм.
Источник
Как создают аккумуляторные батареи
Практически все современные гаджеты объединяет одна деталь — в них есть аккумуляторная батарея. И её ёмкость остаётся одним из главных критериев при выборе устройства. Мы живем в эру мобильности, и требования к аккумуляторам растут с каждым годом.
Батареи для ноутбуков (и многие другие) состоят из энергетических элементов, скомпонованных в связанные друг с другом ячейки. Ноутбуки, как и большая часть других мобильных устройств, работают на литий-ионных или литий-полимерных аккумуляторах.
Мало кто задумывается о том, как сложно создать аккумуляторную батарею, отвечающую требованиям времени. Сегодня вы узнаете, как их производят в промышленных масштабах… начиная с химических элементов.
Li-ion — литий-ионные
Широко распространённый литий-ионный аккумулятор состоит из электродов (катода из алюминиевой фольги и анода из медной), разделенных пористым сепаратором, пропитанным жидким электролитом. Пакет электродов помещен в герметичный корпус, катоды и аноды подсоединены к клеммам-токосъемникам. Корпус иногда оснащают предохранительным клапаном, сбрасывающим внутреннее давление при аварийных ситуациях или нарушениях условий эксплуатации.
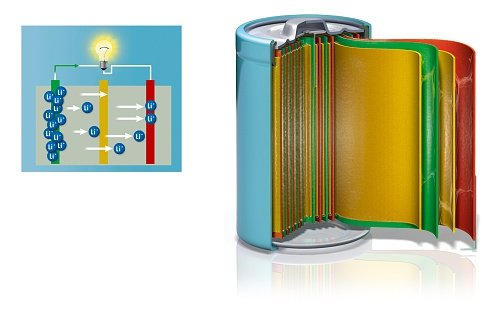
Типичная литий-ионная перезаряжаемая батарея состоит из положительного электрода (зеленый), отрицательного электрода (красный) и разделяющим их слоем сепаратора (желтый). Ионы лития (Li +, синий) перемещаются от отрицательного электрода (анода) к положительному (катод). Во время зарядки происходит обратный процесс, ионы лития переносятся к аноду. Источник
Литий-ионный аккумулятор обладает высокой энергоплотностью, но быстро разряжается при использовании на морозе и может быть взрывоопасен при перезаряде выше 4,2 В. Если вы проколете литий-ионную батарею и создадите короткое замыкание, она загорится и возникнет действительно сильный огонь, который нельзя легко потушить с помощью обычного огнетушителя. Именно поэтому многие такие аккумуляторы оснащают специальной защитой.
Li-po — литий-полимерные
Литий-полимерный аккумулятор (литий-ионный полимерный аккумулятор) представляет собой усовершенствованную конструкцию литий-ионного аккумулятора. В таком аккумуляторе в качестве электролита используется не жидкость, а сухой полимерный материал (синтетический пластик). В отличие от Li-ion, Li-po безопаснее, может отдавать сильные токи и, благодаря полимерному материалу, может быть какой угодно толщины и формы.
Li-po и технологии
Ноутбук, оснащенный литий-полимерным аккумулятором, поддерживает в 3 раза больше циклов зарядки (то есть служит в 3 раза дольше), чем ноутбук со стандартным литий-ионным аккумулятором.
Эффективность энергопотребления достигается не только за счет химических свойств батареи. Если ноутбук остается подключенным к зарядке, когда аккумулятор уже полностью заряжен, это может привести к ухудшению рабочих характеристик аккумулятора и, соответственно, к сокращению срока его службы. Это может также стать причиной набухания аккумулятора из-за внутреннего накопления газов, вызванного окислением, а значит и деформированию или повреждению ноутбука. Дополнительные программные технологии позволяют установить предельный уровень заряда 60%, 80% или 100%, чтобы продлить срок службы батареи и уменьшить вероятность ее набухания.
Ноутбуки также оснащаются механизмом быстрой зарядки, с помощью которого аккумулятор заряжается за несколько десятков минут чуть более чем наполовину.
Li-po vs Li-ion
Положительные и отрицательные электроды Li-po и Li-ion имеют сходный химический состав. Основное различия между двумя видами батарей заключается в способе их компоновки. С литий-ионной технологией для оболочки можно выбрать только жесткий металлический корпус, в то время как литий-полимерная технология позволяет использовать мягкую оболочку для корпуса (пластиковая или алюминиевая фольга). При толщине до 3 мм Li-po имеет преимущество в емкости. При толщине более 3 мм Li-ion дает существенную выгоду в цене.
Существуют и другие виды аккумуляторов на основе лития: LiFePO4 — литий-железо-фосфатные, LiFeYPO4 — литий-железо-иттрий-фосфатные, и другие. Отличаются они различными добавками, улучшающими характеристики батареи. Однако в основе большей части новых экспериментов лежит всё тот же металл, пришедший на смену некогда популярным никель-кадмиевым и никель-металлгидридным аккумуляторам.
Литий

Очень легкий, очень мягкий металл серебристо-белого цвета.
Первые работы в области создания перезаряжаемого аккумулятора на основе лития были начаты в 1912 году, но до 1970-х эксперименты не выходили за пределы лабораторий из-за нестабильности лития. В 1980-х на основе технологий, разработанных в Оксфордском университете, стали появляться первые промышленные литиевые аккумуляторные батареи, которые быстро перегревались и выходили из строя. Только в 1991 году был создан аккумулятор, в котором металлический литий был заменен более безопасной ионной формой.
Литий снискал заслуженную популярность за счет своих особых свойств. Это один из самых легких металлов в периодической таблице, который действительно помогает сохранять большие объемы энергии в небольшом объеме и при незначительном весе. Однако популярность лития сегодня может привести к исчерпанию этого металла в будущем.
Добыча лития — это трудоемкий процесс даже в тех регионах, где металла много. На протяжении десятилетий коммерческое производство лития основывалось на минеральных рудных источниках, таких как сподумен, петалит и лепидолит. Однако извлечение лития из руды вдвое превышает стоимость производства из соляных растворов.
Основные залежи лития, пригодные для активной разработки, находятся в Южной Америке и Китае. На территории России больше всего лития содержится в слюде, сопровождающей месторождения редкоземельных металлов. До недавнего времени добыча лития из слюды стоила слишком дорого, но в 2017 году ученые НИТУ «МИСиС» представили установку, сделавшую добычу соединений лития из бедной руды вдвое дешевле.
Большая часть лития сегодня добывается из естественных водяных линз соляных озер, в насыщенных соляных растворах которых концентрируется хлорид лития, калий и натрий. Раствор выкачивается и выпаривается на солнце, полученная смесь солей перерабатывается.
Извлечение лития

Солончак Уюни содержит около 100 миллионов тонн лития, или от 50 до 70% его мировых запасов.
Крупнейший источник лития находится в Боливии — это солончак Уюни, высохшее соленое озеро, расположенное на высоте около 3650 м над уровнем моря. Имеет площадь 10 588 км². Внутренняя часть покрыта слоем поваренной соли толщиной 2-8 м. Хлорид лития, находящийся здесь в огромных количествах, пригоден для добычи из него лития, а раньше использовался в качестве замены обычной соли. Употреблять в пищу его перестали после открытия токсических эффектов.

Литиевый соляной пруд в Аргентине.
Для извлечения лития соляные растворы сначала перекачивают на поверхность в специальные пруды, где под воздействием солнца в течение нескольких месяцев происходит медленное испарение. Когда хлорид лития в испарительных прудах достигает оптимальной концентрации, раствор перекачивают на восстановительную установку, где фильтрацией удаляют из смеси нежелательные примеси.
Преобразование лития в металл производится в электролитической ячейке. Хлорид лития смешивается с хлоридом калия в соотношении 55% к 45% для того, чтобы произвести расплавленный эвтектический электролит. Далее электролизом расплава при температуре 600 °C получают расплавленный литий, который поднимается на поверхность электролита.
Другие химические элементы
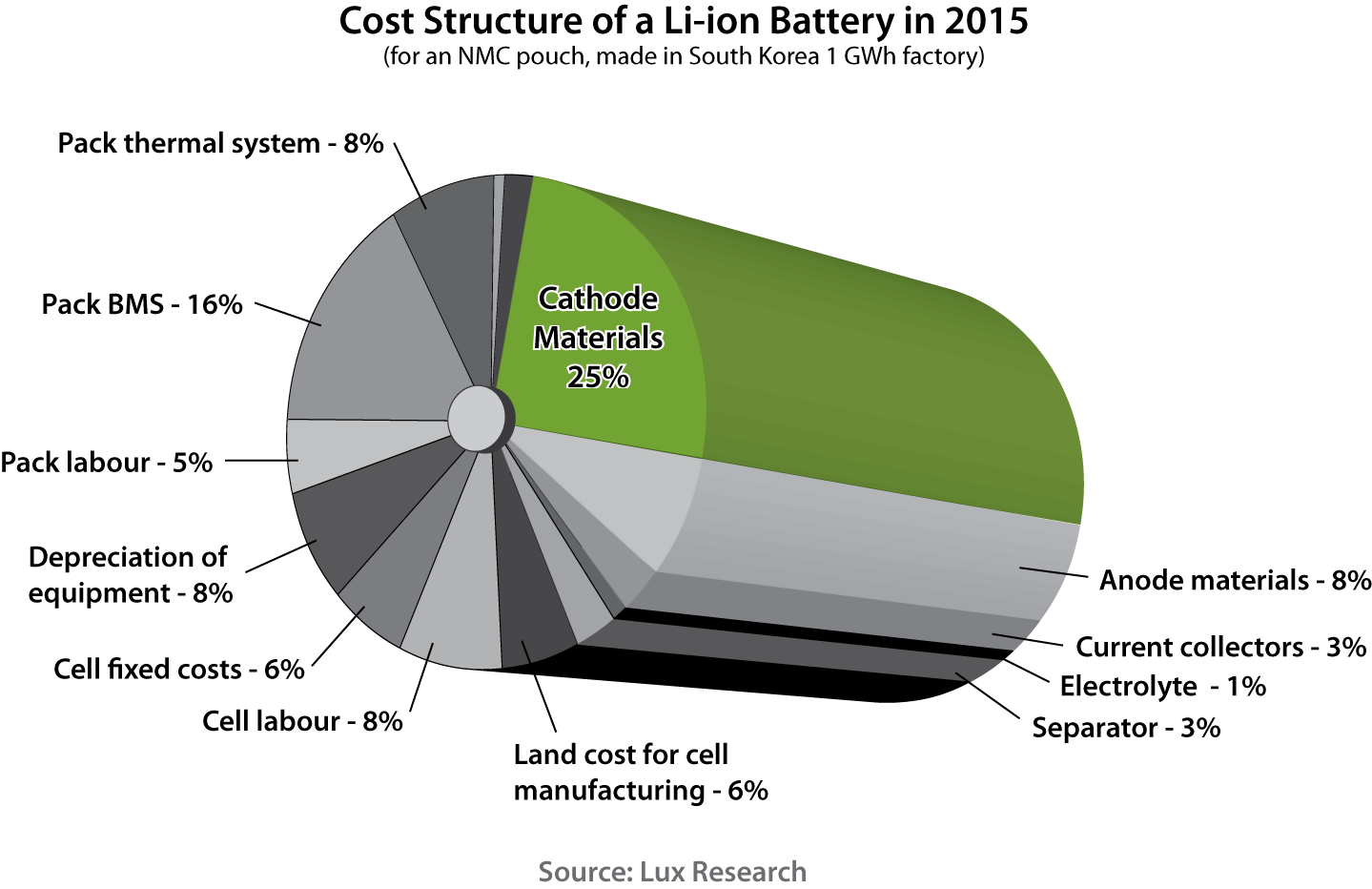
Составляющие стоимости Li-ion батареи.
Внутри литий-ионного аккумулятора может использоваться несколько материалов для катодов. Первоначально основным компонентом катода был кобальт, но он имеет ограниченную доступность в природе и токсичен, что является огромным недостатком для массового производства. Сегодня кобальт частично замещается никелем, а также смесью кобальта, никеля и марганца.
Безопасная и долговечная батарея нуждается в надежном электролите, который может выдерживать существующее напряжение и высокие температуры и имеет длительный срок хранения, обеспечивая высокую подвижность ионов лития. Растворы электролита состоят из органических растворителей, соли LiPF6 (гексафторфосфат лития) и различных добавок.
Электролит высокой чистоты играет ключевую роль в транспортировке положительных ионов лития между катодом и анодом. Электролитные добавки улучшают стабильность, предотвращая деградацию раствора. Состав электролитов варьируется в зависимости от используемых анодных и катодных материалов, однако выбор электролита часто подразумевает компромисс между воспламеняемостью и электрохимическими характеристиками.
Полимерные электролиты представляют собой ионно-проводящие полимеры. Они часто смешиваются в композитах с керамическими наночастицами, что приводит к более высокой проводимости и устойчивости к более высоким напряжениям.
В литий-ионных батареях в качестве токоприемников используется разнообразная металлическая фольга — медная, никелевая или фольга из каталитической меди. Как правило, медная фольга ставится в качестве отрицательного электрода для коллектора анодного тока, а алюминиевая фольга применяется в качестве положительного электрода для катодного токосъемника.

Строение Li-po батареи
Анод состоит из смеси графита и лития (возможно также использование интерметаллидов или кремния), в то время как катод объединяет литий и другие металлы (материалы катода требуют чрезвычайно высокой чистоты и должны быть почти полностью очищены от нежелательных металлических примесей — железа, ванадия и серы).
Отделяет катод от анода сепараторный материал из полипропилена, полиэтилена или другого схожего полимерного материала. Сепараторы большинства батарей состоят из очень простых пластиковых пленок, которые имеют правильный размер пор, чтобы позволить ионам перемещаться, блокируя при этом другие элементы. В случае жидкого электролита сепаратор представляет собой вспененный материал, который пропитывается электролитом и удерживает его на месте.
Процесс производства батареи
Основы для анода и катода поставляются на завод в виде черного порошка, и для неподготовленного глаза они почти неотличимы друг от друга. Порошок очень мелкой фракции, чтобы достичь максимальной эффективной площади поверхности электродов. Форма частиц также важна. Предпочтительны гладкие сферические крупицы с закругленными краями, поскольку острые кромки или шелушащиеся поверхности чувствительны к высоким электрическим нагрузкам.
Аноды и катоды в литиевых батареях имеют одинаковую форму и выполняются по аналогичным процессам на идентичном оборудовании. Но поскольку загрязнение между анодным и катодным материалами приведет к разрушению батареи, то для предотвращения контакта материалов их обычно обрабатываются в разных цехах.
Первая стадия производства заключается в смешивании материалов электродов и нанесении суспензии на поверхность фольги. Активные электродные материалы покрываются с обеих сторон металлической фольгой, которая действует как токоприемник, проводящий ток внутри и снаружи ячейки. Затем фольга с материалами сушится, разрезается на узкие полоски и сворачивается в несколько слоев. Это требует постоянного контроля, поскольку любые заусенцы на краях полосок фольги могут привести к внутренним коротким замыканиям в ячейках.
В процессе сборки батареи сепаратор зажимают между анодом и катодом. После помещения батареи в корпус ее заполняют электролитом и запечатывают. Это должно выполняться в «сухой комнате», так как электролит реагирует с водой. Влага приведет к разложению электролита с выбросом токсичных газов.

Электроды помещают в корпус, оставляя отверстие для добавления электролита/
Как только сборка ячейки будет завершена, она должна пройти хотя бы один контролируемый цикл зарядки/разрядки. Процесс зарядки начинается с низкого напряжения, которое постепенно нарастает. Только после прохождения теста батарея покинет завод и отправится дальше.
В будущем, несомненно, появятся новые виды аккумуляторов. Возможно, тогда литий останется в прошлом. Пока же есть еще множество возможностей для улучшения характеристик существующих аккумуляторных батарей.
Источник











