- Как устроен Li-Ion аккумулятор?
- Как устроена литий-ионная батарея?
- Типы Li-ionаккумуляторов
- Как работает литиевый аккумулятор?
- Особенности зарядкиLi-ionэлементов
- Защита литиевых аккумуляторов
- Производство литиевых элементов питания
- «Литий-ионный»: великая путаница в аккумуляторах
- Для чего литий-ионному аккумулятору разные аноды, катоды, электролит?
- Какие материалы входят в состав литий-ионного аккумулятора?
Как устроен Li-Ion аккумулятор?
Автономную работу всевозможных устройств,отмобильных гаджетов до персонального электротранспорта, обеспечивают аккумуляторы. С учетом необходимых значений емкости и напряжения, они объединяются в аккумуляторные батареи. Ключевые характеристики АКБ – емкость, напряжение, масса, время восполнения заряда, допустимый температурный режим – зависят от типа используемой химии.
Для автономного питания современной техники успешно используются литий-ионные аккумуляторы. Они имеют большой циклический ресурс, малый саморазряд, широкий температурный диапазон и солидную удельную емкость. Катод у таких элементов выполнен из производных лития, а заряд переносят ионы Li. Далее мы подробнее рассмотрим устройство Li-ion аккумуляторов и принцип их работы.
Как устроена литий-ионная батарея?
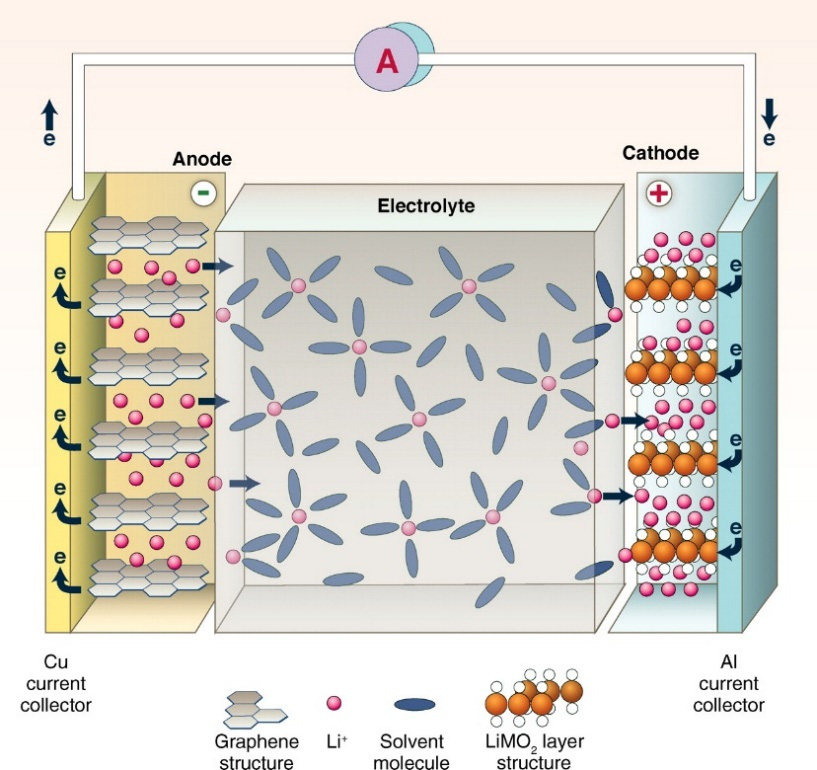
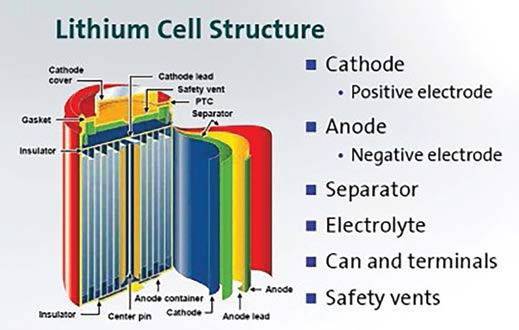
В основе конструкции литий-ионного аккумулятора– 2 составляющие: анод, выполненный из пористого углерода на фольге из меди, и катод – из оксида лития на фольге из алюминия. Их разделяет пористый сепаратор из полипропилена, обильно пропитанный электролитом, который выполняет функции проводника. Система находится в герметичном корпусе. Электроды подключены к токосъемникам. Некоторые аккумуляторы дополнительно имеют клапан-предохранитель для сброса внутреннего давления.
Пластины из меди и алюминия, смазанные электролитом и разделенные пористой прослойкой, обычно сворачиваются в рулон. В итоге получается элемент цилиндрической формы. При другом способе укладки пластин получаются изделия в форме призм и пакетов. Состав катода бывает разным: LiMn2O4, LiFePO4, LiCoO2,LiMnO2, LiMnRON, LiC6, LiNiO2и т.д.
Типы Li-ionаккумуляторов
В зависимости от используемого материала катода литиевые элементы бывают:
- Литий-марганцевые (LiMn2O4, LNO). Имеют меньшее внутреннее сопротивление, высокую мощность и умеренную емкость – 100–150 Вт·ч/кг. Стандартные токи заряда и разряда – до 1С, но есть модели с С-рейтингом зарядки до 3С и С-рейтингом разряда до 10С, а в импульсном режиме – до 50С. Ресурс – около 500 циклов. Применяются такие накопители в электроинструменте, силовых агрегатах, медицинском оборудовании.
- Литий-кобальтовые (LiCoO2, LCO). Имеют высокую энергоемкость (150–200 Вт·ч/кг), но уступают аналогам по термической стабильности и сроку службы (500–1000 циклов). Токи заряда и разряда для таких элементов не должны превышать 1С. Накопители энергии на основе кобальта встречаются все реже, но еще используются в мобильных телефонах, цифровых камерах, ноутбуках.
- Литий-никель-марганец-кобальт-оксидные (NMC, NCM). Обеспечивают высокую мощность и емкость – 150–220 Вт·ч/кг, выдерживают 1000–2000 циклов. Стандартные токи заряда и разряда – 1С. Используются в медицинском и промышленном оборудовании, электровелосипедах и других видах электротранспорта.
- Литий-никель-кобальт-алюминий-оксидные (NCA). Отличаются высокой удельной энергоемкостью – 200–260 Вт·ч/кг. Имеют ресурс около 500 циклов, зарядные токи 0,7С и разрядные 1С. Обеспечивают автономное питание промышленного и медицинского оборудования, электрических силовых агрегатов и других устройств, требующих высокой емкости.
- Литий-железо-фосфатные (LFP, LiFePO4). Отличаются большим ресурсом (более 2000 циклов), термической и химической стабильностью, высокой безопасностью эксплуатации и малым внутренним сопротивлением. Их удельная энергоемкость составляет 90–120 Вт·ч/кг, ток зарядки – 1С, ток разрядки – до 25С. Используются такие элементы питания в устройствах, для которых важна выносливость аккумов, способность работать на морозе и выдерживать высокие токи нагрузки.
- Литий-титанатные (LiTi). Отличаются низким номинальным напряжением (2,4 В) и удельной энергоемкостью 70–80 Вт·ч/кг, но быстро заряжаются, имеют широкий температурный диапазон и ресурс 3000–7000 циклов. Номинальные токи зарядки 1С, максимум – 5С. Допустимые разрядные токи – 10С, а при импульсной подзарядке – 30С. Литий-титанатные элементы считаются самыми безопасными. Используются они в уличном освещении, ИБП, электротранспорте.
Как работает литиевый аккумулятор?
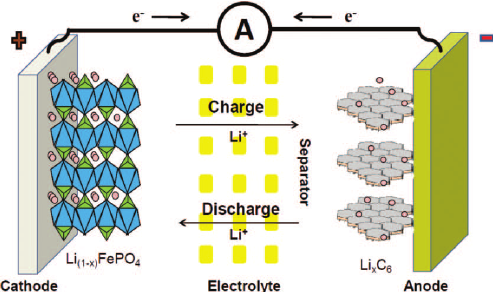
Принцип работы Li-ion аккумуляторов идентичен для элементов всех типов, независимо от материала катода.Когда на электроды подается напряжение – «плюс» на оксид лития и «минус» на графит – положительно заряженные ионы лития отцепляются от молекул оксида и переходят на углеродную пластинку. В результате протекает окислительная реакция, и аккумулятор заряжается.
При работе литиевого аккумулятора под нагрузкой протекает обратный процесс. Ионы Li + возвращаются на пластинку из оксида лития, в свое стандартное состояние. Графитовая пластинка на фольге из меди становится «минусом», а оксид лития на фольге из алюминия – «плюсом».
Особенности зарядкиLi-ionэлементов
Литий-ионные элементы питания чувствительны к перезаряду. На поверхности анода при чрезмерном заряде осаждается металлический литий. Он выглядит как мелкий мшистый осадок и способен вступать в реакцию с электролитом. На катоде при перезаряде активно выделяется кислород. Внешне это может проявляться в виде интенсивного нагрева, роста давления и разгерметизации элемента.
Заряжаются Li-ionаккумуляторы в 2 этапа:
- При стабильном значении тока 0,2С–1С до рекомендованного производителем напряжения, обычно – 4,1–4,2 В. Длится эта стадия около 40 минут.
- При неизменном напряжении. Процесс зарядки завершается, когда значение зарядного тока уменьшается до величины, составляющей 3% от начального значения.
Быстрее происходит зарядка в импульсном режиме.Но для продления срока службы литиевых элементов их рекомендуется заряжать током, номинал которого составляет 50% от значения емкости, т.е. 0,5С.
Защита литиевых аккумуляторов
Элементы питания на основе лития защищены от коротких замыканийвнутри системы, например, с помощью 2-слойного сепаратора. Один из его слоев выполняется не из полипропилена, а из аналога полиэтилена. При риске короткого замыкания, к примеру, если дендриты лития прорастают к катоду, защитный слой локально нагревается, частично плавится, становится непроницаемым и блокирует последующее прорастание дендритов.
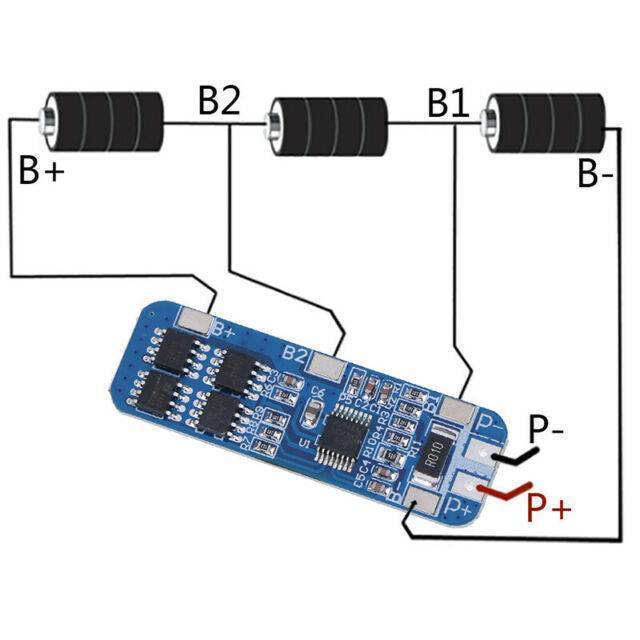
Для защиты от избыточного заряда и глубокого разряда накопители энергии снабжаются специальными ограничителями – платами защиты по току и напряжению. Они не допускают выхода напряжения за границы рекомендованного диапазона и в критических ситуациях автоматически отключают элемент от питания или нагрузки.
Поэтому для безопасной работы элементов и аккумуляторных батарей важно использовать BMSплаты. В противном случае высок риск повреждения аккумуляторов и их преждевременного выхода из строя. Такой контроллер зарядно-разрядного процесса может устанавливаться и на отдельные аккумуляторы, и на собранную из них батарею.
Производство литиевых элементов питания
Сырье для основных элементов в схеме Li-ion аккумуляторов – катода и анода – имеет вид мелкофракционного черного порошка. Чем мельче частицы, тем больше получается эффективная площадь электродов. Оптимальная форма частиц – сферическая, с гладкими краями, т.к. неровности чувствительны к токовым нагрузкам.
Производственный процесс состоит из следующих этапов:
- Порошковидные материалы наносятся в виде суспензии на фольгу. Аноды и катоды обычно производятся в различных цехах, чтобы обеспечить максимальную чистоту материалов. Металлическая фольга играет роль токоприемника.
- Фольга с нанесенными материалами сушится, разделяется на полоски и складывается в несколько слоев. Процесс сворачивания строго контролируется, т.к. любые дефекты способны привести к коротким замыканиям внутри системы.
- Между пластинами анода и катода зажимается сепаратор, обработанный электролитом.
- Пластинки сворачиваются рулоном или по другой схеме и помещаются в корпус.
Готовые изделия проходят тестирование – контролируемый цикл заряда-разряда. Подзарядку начинают с минимального напряжения и с постепенным его повышением.Протестированные изделия заряжаются до оптимального уровня, чтобы исключить риск значительного падения напряжения из-за саморазряда, и поставляются в продажу.
Предыдущая статья нашего блога посвящена сигнализации для электровелосипедов.
Источник
«Литий-ионный»: великая путаница в аккумуляторах
Литий-ионный аккумулятор (Li-Ion Battery) — объединяющее название всех аккумуляторов литий-ионного типа с разными материалами анода, катода и составами электролита.
Всё будет просто до тех пор, пока вы не услышите литий-титанат и литий-железо-фосфат , а потом не начнёте сравнивать литий-ионный с литий-полимерным . Как развязать клубок путаницы в этих названиях?
Если вы слышите о литий-кобальтовом аккумуляторе , то знайте, что это самый обыкновенный и наиболее распространённый литий-ионный аккумулятор из наших с вами смартфонов. Почему он « кобальтовый »? Из-за кобальта на его катоде.
👍 По маркетинговому названию производители могут понимать особенности конкретной ячейки.
Или, например, зная о преимуществах кремниевых анодов аккумуляторов , в самых массовых литий-кобальтовых ячейках можно добиться лучшей ёмкости, чем с традиционным графитовым анодом. В проект смартфона инженером будет закладываться уже литий-кобальтовый аккумулятор с кремниевым анодом .
Теперь разберёмся подробнее.
Для чего литий-ионному аккумулятору разные аноды, катоды, электролит?
Для чего им разные материалы? У одной химии больше пользы в безопасности или ёмкости (увеличена плотность энергии), у другой лучше получится удерживать заряд в мороз или увеличить ток разряда (актуально в электроинструменте или электромобилях ).
💡 При выборе анода, катода, электролита многое зависит от назначения самого электронного устройства.
Например, в смартфонах нужны батареи:
- компактные (толстые и тяжёлые гаджеты не покупают — почему );
- максимально ёмкие (чтобы держал заряд весь день, а лучше два);
- максимально дешёвые (в масштабном производстве каждый рубль имеет значение).
Ради этого можно пожертвовать определёнными характеристиками:
- сроком службы (количества циклов достаточно для двух-трёх лет эксплуатации, ведь к тому моменту смартфон морально устаревает);
- предиктивной безопасностью (толстый прочный корпус не нужен — его заменяет корпус смартфона, да и выполнять контроль лучше более «умными» программно-аппаратными средствами).
К литий-ионной аккумуляторной ячейке в компактном размере, ёмкой с приемлемым сроком службы и базовой безопасностью как раз идеально подходит кобальтовый катод (LiCoO2, LCO) в тандеме с графитовым анодом. Недорогой в производстве, быстро изготавливается, массовый продукт.
💡 Но ведь есть устройства, где срок службы и безопасность куда важнее цены и ёмкости.
Например? Источники бесперебойного питания. Мы в подробностях рассказывали как раз о таких надёжных батареях — литий-железо-фосфатных (LiFePo4, LFP).
Служат больше 10 лет, высокий ток разряда, выдерживают термические потрясения, беспрецедентно для литий-ионной технологии стабильны даже при коротком замыкании. Но всё ещё слишком дорого стоят за ту же ёмкость, что и LCO .
О «гаджетовой» компактности LiFePo4 при этом можно забыть. Если только сравнивать их со свинцово-кислотными АКБ из наших с вами автомобилей. Потому они лучше подходят как раз для ИБП (безопаснее, работают более 10 лет, не нужно обслуживать).
Источник
Какие материалы входят в состав литий-ионного аккумулятора?
Современные катодные материалы включают оксиды лития-металла [такие как LiCoO2, LiMn2O4, и Ли (NixMnyCoz) O2], оксиды ванадия, оливины (такие как LiFePO4), и перезаряжаемые оксиды лития. 11,12 Слоистые оксиды, содержащие кобальт и никель, являются наиболее изученными материалами для литий-ионных аккумуляторов. Они демонстрируют высокую стабильность в диапазоне высокого напряжения, но кобальт имеет ограниченную доступность в природе и токсичен, что является огромным недостатком для массового производства. Марганец предлагает недорогую замену с высоким тепловым порогом и отличными скоростными характеристиками, но ограниченными циклическими характеристиками. Поэтому часто используются смеси кобальта, никеля и марганца, чтобы объединить лучшие свойства и минимизировать недостатки. Оксиды ванадия обладают большой емкостью и отличной кинетикой. Однако из-за введения и извлечения лития материал имеет тенденцию становиться аморфным, что ограничивает циклическое поведение. Оливины нетоксичны и обладают умеренной способностью к выцветанию из-за цикличности, но их проводимость низкая. Были внедрены методы покрытия материала, которые компенсируют плохую проводимость, но это увеличивает стоимость обработки батареи.
Материалы анода — это литий, графит, легирующие литий материалы, интерметаллиды или кремний. 11 Литий кажется наиболее простым материалом, но имеет проблемы с циклическим поведением и ростом дендритов, что создает короткие замыкания. Углеродистые аноды являются наиболее часто используемым анодным материалом из-за их низкой стоимости и доступности. Однако теоретическая емкость (372 мАч / г) оставляет желать лучшего по сравнению с плотностью заряда лития (3,862 мАч / г). Некоторые попытки с новыми разновидностями графита и углеродными нанотрубками были направлены на увеличение емкости, но это было связано с высокими затратами на обработку. Аноды из сплавов и интерметаллические соединения обладают высокой емкостью, но также демонстрируют резкое изменение объема, что приводит к плохому циклическому поведению. Были предприняты попытки преодолеть изменение объема за счет использования нанокристаллических материалов и наличия фазы сплава (с Al, Bi, Mg, Sb, Sn, Zn и другими) в нелегирующей стабилизационной матрице (с Co, Cu, Fe или Ni). Кремний имеет чрезвычайно высокую емкость 4,199 мАч / г, что соответствует составу Si.5Li22. Тем не менее, циклическое поведение плохое, а снижение емкости еще не изучено.
Безопасная и долговечная батарея нуждается в прочном электролите, который может выдерживать существующее напряжение и высокие температуры и который имеет длительный срок хранения, предлагая высокую подвижность для ионов лития. Типы включают жидкие, полимерные и твердотельные электролиты. 11 Жидкие электролиты — это в основном органические электролиты на основе растворителей, содержащие LiBC.4O8(LiBOB), LiPF6, Ли [ПФ3(C2F5)3], или похожие. Наиболее важным фактором является их воспламеняемость; самые эффективные растворители имеют низкие температуры кипения и температуры вспышки около 30 ° C. Следовательно, выброс или взрыв элемента, а затем и аккумулятора представляют опасность. Разложение электролита и высокоэкзотермические побочные реакции в литий-ионных батареях могут вызвать эффект, известный как «тепловой разгон». Таким образом, выбор электролита часто включает компромисс между воспламеняемостью и электрохимическими характеристиками.
Сепараторы имеют встроенные механизмы теплового отключения, а к модулям и аккумуляторным блокам добавляются дополнительные внешние сложные системы управления температурой. Рассматриваются ионные жидкости из-за их термической стабильности, но они имеют серьезные недостатки, такие как растворение лития из анода.
Полимерные электролиты — это полимеры с ионной проводимостью. Их часто смешивают в композитах с керамическими наночастицами, что приводит к более высокой проводимости и устойчивости к более высоким напряжениям. Кроме того, из-за своей высокой вязкости и квазитвердого поведения полимерные электролиты могут препятствовать росту дендритов лития. 13 и поэтому может использоваться с анодами из металлического лития.
Твердые электролиты представляют собой литий-ионные проводящие кристаллы и керамические стекла. Они показывают очень плохие низкотемпературные характеристики, поскольку подвижность лития в твердом веществе значительно снижается при низких температурах. Кроме того, твердые электролиты требуют особых условий осаждения и температурной обработки для получения приемлемого поведения, что делает их чрезвычайно дорогими в использовании, хотя они устраняют необходимость в сепараторах и риск теплового разгона.
Хороший обзор материалов и потребностей сепараторов представлен П. Арора и З. Чжан. 14 Как следует из названия, разделитель батарей физически отделяет два электрода друг от друга, что позволяет избежать короткого замыкания. В случае жидкого электролита сепаратор представляет собой вспененный материал, пропитанный электролитом и удерживающий его на месте. Это должен быть электронный изолятор, обладающий минимальным электролитическим сопротивлением, максимальной механической стабильностью и химической стойкостью к разложению в высоко электрохимически активной среде. Кроме того, сепаратор часто имеет функцию безопасности, называемую «тепловым отключением»; при повышенных температурах он плавится или закрывает поры, чтобы отключить литий-ионный транспорт без потери своей механической стабильности. Сепараторы либо синтезируются в листах и собираются с электродами, либо наносятся на один электрод на месте. С точки зрения затрат последний метод является предпочтительным, но создает некоторые другие проблемы синтеза, обращения и механики. Твердотельные электролиты и некоторые полимерные электролиты не нуждаются в сепараторе.
Источник