- Гальванические элементы и аккумуляторы — устройство, принцип работы, виды
- Химические источники тока. Виды и особенности. Устройство и работа
- Устройство и работа
- Химические источники тока состоят из электродов и электролита, который находится в емкости. Электрод, на котором окисляется восстановитель, называется анодом. Электрод, на котором восстанавливается окислитель, называется катодом. В общем получается электрохимическая система.
- Из чего состоят химические источники тока
Гальванические элементы и аккумуляторы — устройство, принцип работы, виды
Маломощные источники электрической энергии
Для питания переносной электро- и радиоаппаратуры применяют гальванические элементы и аккумуляторы.
Гальванические элементы — это источники одноразового действия, аккумуляторы — источники многоразового действия.
Простейший гальванические элемент
Простейший элемент может быть изготовлен из двух полосок: медной и цинковой, погруженных в воду, слегка подкисленную серной кислотой. Если цинк достаточно чист, чтобы быть свободным от местных реакций, никаких заметных изменений не произойдет до тех пор, пока медь и цинк не будут соединены проводом.
Однако полоски имеют разные потенциалы одна по отношению к другой, и когда они будут соединены проводом, в нем появится электрический ток. По мере этого действия цинковая полоска будет постепенно растворяться, а близ медного электрода будут образовываться пузырьки газа, собирающиеся на его поверхности. Этот газ — водород, образующийся из электролита. Электрический ток идет от медной полоски по проводу к цинковой полоске, а от нее через электролит обратно к меди.
Постепенно серная кислота электролита замещается сульфатом цинка, образующимся из растворенной части цинкового электрода. Благодаря этому напряжение элемента уменьшается. Однако еще более сильное падение напряжения вызывается образованием газовых пузырьков на меди. Оба эти действия производят «поляризацию». Подобные элементы не имеют почти никакого практического значения.
Важные параметры гальванических элементов
Величина напряжения, даваемого гальваническими элементами, зависит только от их типа и устройства, т. е. от материала электродов и химического состава электролита, но не зависит от формы и размеров элементов.
Сила тока, которую может давать гальванический элемент, ограничивается его внутренним сопротивлением.
Очень важной характеристикой гальванического элемента является электрическая емкость. Под электрической емкостью подразумевается то количество электричества, которое гальванический или аккумуляторный элемент способен отдать в течение всего времени своей работы, т. е. до наступления окончательного разряда.
Отданная элементом емкость определяется умножением силы разрядного тока, выраженной в амперах, на время в часах, в течение которого разряжался элемент вплоть до наступления полного разряда. Поэтому электрическая емкость выражается всегда в ампер-часах (А х ч).
По величине емкости элемента можно также заранее определить, сколько примерно часов он будет работать до наступления полного разряда. Для этого нужно емкость разделить на допустимую для этого элемента силу разрядного тока.
Однако электрическая емкость не является величиной строго постоянной. Она изменяется в довольно больших пределах в зависимости от условий (режима) работы элемента и конечною разрядного напряжения.
Если элемент разряжать предельной силой тока и притом без перерывов, то он отдаст значительно меньшую емкость. Наоборот, при разряде того же элемента током меньшей силы и с частыми и сравнительно продолжительными перерывами элемент отдаст полную емкость.
Что же касается влияния на емкость элемента конечного разрядного напряжения, то нужно иметь в виду, что в процессе разряда гальванического элемента его рабочее напряжение не остается на одном уровне, а постепенно понижается.
Распространенные виды гальванических элементов
Наиболее распространены гальванические элементы марганцево-цинковой, марганцево-воздушной, воздушно-цинковой и ртутно-цинковой систем с солевым и щелочным электролитами. Сухие марганцево-цинковые элементы с солевым электролитом имеют начальное напряжение от 1,4 до 1,55 В, продолжительность работы при температуре окружающей среды от -20 до -60 о С от 7 ч до 340 ч.
Сухие марганцево-цинковые и воздушно-цинковые элементы со щелочным электролитом имеют напряжение от 0,75 до 0,9 В и продолжительность работы от 6 ч до 45 ч.
Сухие ртутно-цинковые элементы имеют начальное напряжение от 1,22 до 1,25 В и продолжительность работы от 24 ч до 55 ч.
Наибольший гарантийный срок хранения, достигающий 30 месяцев, имеют сухие ртутно-цинковые элементы.
Аккумуляторы — это вторичные гальванические элементы. В отличие от гальванических элементов в аккумуляторе же сразу после сборки никакие химические процессы не возникают.
Чтобы в аккумуляторе начались химические реакции, связанные с движением электрических зарядов, нужно соответствующим образом изменить химический состав его электродов (а частью и электролита). Это изменение химического состава электродов происходит под действием пропускаемого через аккумулятор электрического тока.
Поэтому, чтобы аккумулятор мог давать электрический ток, его предварительно нужно «зарядить» постоянным электрическим током от какого-нибудь постороннего источника тока.
От обычных гальванических элементов аккумуляторы выгодно отличаются также тем, что после разряда они опять могут быть заряжены. При хорошем уходе за ними и при нормальных условиях эксплуатации аккумуляторы выдерживают до нескольких тысяч зарядов и разрядок. 
В настоящее время наиболее часто на практике применяют свинцовые и кадмиево-никелевые аккумуляторы. У первых электролитом служит раствор серной кислоты, а у вторых — раствор щелочей в воде. Свинцовые аккумуляторы называют также кислотными, а кадмиево-никелевые — щелочными.
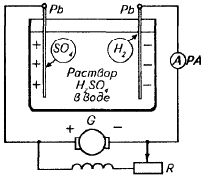
Принцип работы аккумуляторов основан на поляризации электродов при электролизе. Простейший кислотный аккумулятор устроен следующим образом: это две свинцовые пластины, опущенные в электролит. В результате химической реакции замещения пластины покрываются слабым налетом сернокислого свинца PbSO4, как это следует из формулы Pb + H2SO4 = PbSO4 + Н2.
Устройство кислотного аккумулятора
Такое состояние пластин соответствует разряженному аккумулятору. Если теперь аккумулятор включить на заряд, т. е. подсоединить его к генератору постоянного тока, то в нем вследствие электролиза начнется поляризация пластин. В результате заряда аккумулятора его пластины поляризуются, т. е. изменяют вещество своей поверхности, и из однородных (PbSO4) превращаются в разнородные (Pb и Р b О 2 ).
Аккумулятор становится источником тока, причем положительным электродом у него служит пластина, покрытая двуокисью свинца, а отрицательным — чистая свинцовая пластина.
К концу заряда концентрация электролита повышается вследствие появления в нем дополнительных молекул серной кислоты.
В этом одна из особенностей свинцового аккумулятора: его электролит не остается нейтральным и сам участвует в химических реакциях при работе аккумулятора.
Как зарядить аккумулятор
Существует несколько способов заряда аккумуляторов. Наиболее простой — нормальный заряд аккумулятора, который происходит следующим образом. Вначале на протяжении 5 — 6 ч заряд ведут двойным нормальным током, пока напряжение на каждой аккумуляторной банке не достигнет 2,4 В.
Нормальный зарядный ток определяют по формуле I зар = Q/16
где Q — номинальная емкость аккумулятора, Ач.
После этого зарядный ток уменьшают до нормального значения и продолжают заряд и течение 15 — 18 ч, до появления признаков конца заряда.
Кадмиево-никелевые, или щелочные аккумуляторы, появились значительно позже свинцовых и по сравнению с ними представляют собой более совершенные химические источники тока. Главное преимущество щелочных аккумуляторов перед свинцовыми заключается в химической нейтральности их электролита по отношению к активным массам пластин. Благодаря этому саморазряд у щелочных аккумуляторов получается значительно меньше, чем у свинцовых. Принцип действия щелочных аккумуляторов также основан на поляризации электродов при электролизе.
Для питания радиоаппаратуры выпускают герметичные кадмиево-никелевые аккумуляторы, которые работоспособны при температурах от -30 до +50 о С и выдерживают 400 — 600 циклов заряд-разряд. Эти аккумуляторы выполняют в форме компактных параллелепипедов и дисков с массой от нескольких граммов до килограммов.
Выпускают никель-водородные аккумуляторы для энергоснабжения автономных объектов. Удельная энергия никель-водородного аккумулятора составляет 50 — 60 Вт ч кг -1 .
Если Вам понравилась эта статья, поделитесь ссылкой на неё в социальных сетях. Это сильно поможет развитию нашего сайта!
Не пропустите обновления, подпишитесь на наши соцсети:
Источник
Химические источники тока. Виды и особенности. Устройство и работа
Химические источники тока (ХИТ) — эта тема имеет высокое практическое значение. Это кардиостимуляторы, электромобили, которые пытаются сохранить экологию, портативные устройства, включая фото и видеотехнику, компьютерную технику, навигаторы. За последние годы прогресс химических источников тока произошел большой, от известных свинцовых аккумуляторов, которые постепенно вытесняются литий-ионными, литий-полимерными и другими аккумуляторами.
В этой области борьба идет за мощность, емкость, которая позволяет максимально долго использовать источники тока. Дополнительным стимулом к их развитию является создание гибких источников тока. Научная составляющая в этой области лежит в плане разработки материалов для таких химических элементов.
Устройство и работа
Химические источники тока состоят из электродов и электролита, который находится в емкости. Электрод, на котором окисляется восстановитель, называется анодом. Электрод, на котором восстанавливается окислитель, называется катодом. В общем получается электрохимическая система.
Попутным результатом такой реакции стало возникновение тока. Восстановитель передает электроны на окислитель, который восстанавливается. Электролит, который находится между электродами, нужен для прохождения реакции. Если перемешать порошки различных двух металлов, то электричество не возникнет, энергия появится в виде теплоты. Электролит необходим для упорядочения процесса движения электронов. Электролит состоит обычно из раствора соли или расплавленного вещества.
Электроды имеют вид решеток или пластин из металла. При помещении их в раствор электролита получается разность потенциалов пластин. Анод отдает электроны, а катод их принимает. На поверхности возникают химические реакции. Когда цепь размыкается, то реакции прекращаются. Если реагенты закончились, то реакция также больше не идет. Если удалить один из электродов, то цепь размыкается.
Из чего состоят химические источники тока
В качестве окислителей применяются соли и кислородосодержащие кислоты, а также нитроорганические вещества, кислород. В качестве восстановителей применяются металлы, оксиды, углеводороды.
Электролит может состоять из:
- Соли, щелочи и кислоты, растворенные в воде.
- Соли в растворе, с возможностью электронной проводимости.
- Расплавленные соли.
- Твердые вещества с подвижным ионом.
- Электролиты в виде матрицы. Это растворы жидкости, расплавы, которые находятся в порах электроносителя.
- Электролиты с ионным обменом. Твердые вещества с закрепленными ионогенными группами, с одним знаком. С другим знаком ионы подвижны. Эта характеристика позволяет создать однополярную проводимость.
Гальванические элементы
Напряжение на ячейке составляет 0,5-4 вольта. В химических образцах источника применяют гальваническую батарею, которая состоит из элементов. Может использоваться параллельная схема нескольких элементов. При последовательной схеме в цепь включены одинаковые батареи. Они должны обладать одинаковыми свойствами, с одной конструкцией, технологией, типоразмером. Для схемы параллельного соединения подойдут элементы с различными свойствами.
Классы
Химические источники тока делятся по следующим свойствам:
- Размерности.
- Конструктивным особенностям.
- Применяемым химическим веществам.
- Источнику реакции.
Эти свойства создают эксплуатационные параметры источников, которые подходят для определенной области использования.
Деление на классы электрохимических источников основывается на отличии в способе действия устройства. По этим свойствам их различают:
- Первичные источники – для однократного применения. В них заключен определенный запас веществ, который будет израсходован при реакции. Когда произойдет разряд, ячейка исчерпывает свою способность к работе. Первичные источники, основанные на химических реакциях, называются элементами. Наиболее простой элемент – это батарейка типа АА.
- Химические источники тока , которые имеют возможность перезаряжаться, называются аккумуляторами, это вторичные многоразовые элементы. Израсходованные химические элементы могут регенерироваться и снова накопить энергию, путем подключения к ним тока. Это называется зарядкой элементов. Такие элементы применяют длительное время, так как их легко зарядить. В процессе разряда вырабатывается электрический ток. К таким источникам можно причислить элементы питания различных видов приборов и устройств, таких как смартфоны, ноутбуки и т.д.
- Тепловые химические источники тока – это приборы постоянного действия. В результате их работы постоянно поступает новая порция веществ и удаляется использованный продукт реакции.
- В смешанных элементах находится запас реагента. Другой реагент поступает в устройство снаружи. Время действия устройства имеет зависимость от резерва первого вещества. Комбинированные элементы применяются в качестве аккумуляторов, когда имеется возможность регенерации их заряда через прохождение тока от внешнего питания.
- Химические источники тока, которые могут возобновлять заряд , заряжаются разными способами. В них можно заменять израсходованные реагенты. Такие источники действуют не постоянно.
Свойства
Основные характеристики ХИТ можно перечислить в таком виде:
- Разрядное напряжение. Это свойство имеет зависимость от определенной электрохимической системы. А также оказывает влияние процент концентрации электролита, температура, ток.
- Мощность.
- Разрядный ток, зависящий от сопротивления цепи.
- Емкость, наибольшее количество энергии, которое источник выдает при общем разряде.
- Запас энергии – наибольшая энергия, которая получена при полном разряде устройства.
- Энергетические свойства и характеристики. Для батарей аккумуляторов это число циклов заряда и разряда, без уменьшения емкости и напряжения (ресурс).
- Температурный интервал работы.
- Сохраняемый срок – наибольший допускаемый период времени от изготовления до первого разряда элемента.
- Время службы – наибольший допускаемый срок работы и хранения. Для элементов на топливе имеют значение сроки работы при постоянной и периодической работе.
- Полная энергия, отданная за все время работы.
- Механическая, вибрационная прочность.
- Возможность функционирования в любом положении.
- Надежная работа.
- Простота в уходе.
Сахарная батарея
Чтобы произвести литий-ионные аккумуляторы в Японии закупают материалы в других странах. Это негативно сказывается на экономическом положении страны. Поэтому ученые ищут способы изготовления аккумуляторов из того сырья, которое имеется в наличии. Таким сырьем в Японии стал сахар. Аккумулятор на сахаре в Японии по свойствам имеет надежность и энергоемкость выше обычных аналогов, и стоимость его ниже.
Большой спрос на литий, который вызван резким распространением переносных аккумуляторов, озаботил производителей аккумуляторов, так как этот элемент добывается только в странах с политической нестабильностью. Это явилось вторым фактором поиска альтернативных материалов для недорогих аккумуляторов с высокой надежностью. Сахароза легко преобразуется в дешевый материал для анодного сырья в литий-ионных батареях.
Сахар нагревают в условиях вакуума под давлением до 1500 градусов. Он превращается в порошок, состоящий из углерода, который может повысить заряд на 20% больше аналогичных изделий. Это явилось первым шагом в разработке дешевых батарей. Пока такие виды батарей не составляют конкуренции современным аккумуляторам. Но ученые предполагают, что в будущем подобные разработки вытеснят дорогие изделия.
Требования
Конструктивные особенности химических источников тока должны создавать условия, которые способствовали бы максимальной эффективности химических реакций.
К таким условиям можно отнести:
- Недопущение утечек тока.
- Постоянная работа.
- Герметичность.
- Раздельное помещение реагентов.
- Качественное контактирование электролита с электродами.
- Хороший отвод тока из объекта химической реакции до наружного вывода с наименьшими потерями.
К химическим элементам предъявляются требования:
- Повышенные значения свойств.
- Максимальный диапазон температуры работы.
- Наибольшее напряжение.
- Минимальная себестоимость электричества.
- Постоянное значение напряжения.
- Хорошее сохранение заряда.
- Безопасное функционирование.
- Простое обслуживание, или ее отсутствие.
- Долговременная работа.
Эксплуатация источников тока
Основное достоинство первичных элементов состоит в отсутствии надобности обслуживания. Перед работой нужно просто осмотреть их, определить срок годности. При включении в цепь нельзя путать полярность и допускать повреждения контактов. Сложные конструкции источников требуют особого ухода. Цель его заключается в удлинении срока службы до максимума.
Уход за аккумуляторами требует выполнения следующих мероприятий:
- Обеспечение чистоты.
- Контроль параметра напряжения отключенной цепи.
- Обеспечение необходимого уровня электролита, доливки дистиллированной воды.
- Проверка концентрации электролита ареометром.
При использовании батареек (гальванических элементов) нужно выполнять требования, которые относятся к применению электрических приборов.
Сфера использования
В современное время химические источники тока используются в:
- Транспорте.
- Переносных устройствах.
- Космической технике.
- Оборудовании научных исследований.
- Медицинских приборах.
Применяются в бытовой сфере:
- Батарейки (сухие).
- Батареи аккумуляторов электроники.
- Аккумуляторы на автомобилях.
Большое распространение нашли литиевые химические источники тока. Это обусловлено наличием у лития максимальной удельной энергии. Он отличается наиболее отрицательным потенциалом электрода из металлов. Батареи литий ионного типа опередили все другие источники по размеру значений удельной энергии. В настоящее время ученые разрабатывают различные усовершенствования литиевых аккумуляторов. Разработки ведутся в направлении получения конструкций корпуса сверхмалой толщины, которые будут использоваться для питания смартфонов и подобных им гаджетов, а также создание сверхмощных батарей аккумуляторов.
В последнее время серьезные работы ученых ведутся по изобретению и модернизации топливных батарей – устройств, которые создают электрическую энергию, за счет проведения химических реакций веществ, постоянно подающихся к электродам снаружи. Для окисления берут кислород, а в качестве топлива пытаются использовать водород. На основе таких батарей уже действуют некоторые опытные образцы на электростанциях.
Источник